|
Chap. N° 10 |
Représentation spatiale des molécules. Cours. |
|
|
|
|
II- Représentation des
molécules organiques. |
|
III- Les différentes relations
de stéréoisomérie.
b)- Stéréoisomčres de conformation :
c)- Stéréoisomčres de configuration. 2)- Stéréoisomérie de configuration : Cas des composés ŕ un atome de carbone asymétrique.
b)- Énantiomérie et propriétés :
3)- Stéréoisomérie de configuration : Cas des composés ŕ deux atomes de carbone asymétrique. 4)- Stéréoisomérie de
configuration : diastéréoisomčres
Z / E. 5)- Stéréoisomérie de
conformation. |
|
Stéréochimie Les molécules ont été réalisées avec Schemsketch  Logiciel Gratuit
Logiciel Gratuit |
|
Exercices : énoncé et correction a)- Exercice 7 page 270 : Reconnaître une molécule chirale. b)- Exercice 8 page 270 : Utiliser la représentation topologique. c)- Exercice 10 page 270 : établir une représentation de Cram. d)- Exercice 15 page 271 : Représenter un couple d’énantiomčres. e)- Exercice 17 page 272 : de la formule semi-développée ŕ la formule
topologique. f)-
Exercice 20 page 272 : La vitamine C. g)- Exercice 22 page 273 : Autour des acides α–aminés. h)- Exercice 28 page 275 : Phéromone sexuelle de coléoptčre. |

- Un objet est chiral s’il n’est pas superposable ŕ son
image dans un miroir.
- La chiralité est la propriété d'un objet de ne pas ętre
superposable ŕ son image dans un miroir.
- Donner un exemple d'un objet chiral. (Une
main)
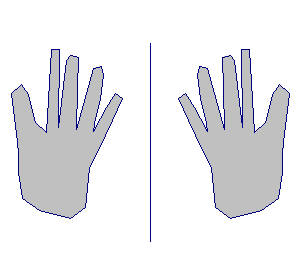
- La chiralité a été étendue aux molécules par PASTEUR en
1848.
2)- La
chiralité au niveau moléculaire.
![]() Construire une molécule
A possédant :
Construire une molécule
A possédant :
![]() Un
carbone tétragonal et quatre groupes différents (prendre une
boule rouge, une
verte, une boule
jaune et une boule blanche).
Un
carbone tétragonal et quatre groupes différents (prendre une
boule rouge, une
verte, une boule
jaune et une boule blanche).
![]() Placer la liaison carbone-boule jaune
verticalement.
Placer la liaison carbone-boule jaune
verticalement.
![]() Mettre la molécule A devant un miroir et
construire la molécule B image de A dans le
miroir.
Mettre la molécule A devant un miroir et
construire la molécule B image de A dans le
miroir.
![]() Représenter les deux molécules
A et B
ŕ l'aide de la représentation conventionnelle.
Représenter les deux molécules
A et B
ŕ l'aide de la représentation conventionnelle.
![]() Les
molécules A et B sont-elles superposables ?
Les
molécules A et B sont-elles superposables ?
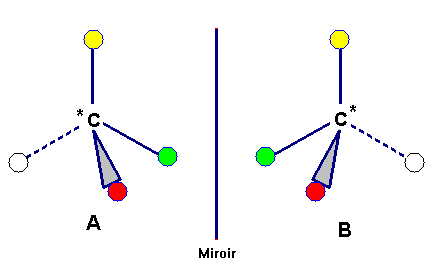
Animation CabriJava
- Les molécules A et B ne sont pas superposables, elles sont image l'une de l'autre dans un miroir.
- Ce sont des
molécules chirales.
- Une molécule est chirale si elle n’est pas superposable ŕ
son image dans un miroir.
II- Représentation des
molécules organiques.
1)-
Formules planes.
► Une molécule peut ętre représentée par :
- Sa formule développée,
- Sa formule semi-développée,
- Sa formule topologique.
- Cours de premičre S. De la structure aux propriétés des alcanes et des alcools
![]() Donner
les représentations de la molécule de butan-2-ol.
Donner
les représentations de la molécule de butan-2-ol.
- Modčle moléculaire :
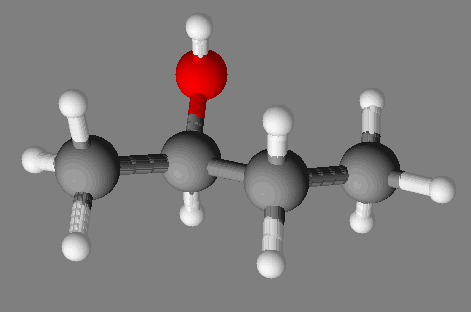
- Formule développée :
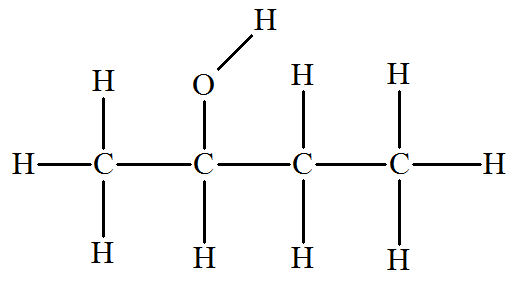
- Formule semi-développée :
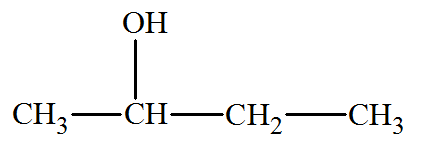
- Formule topologique :
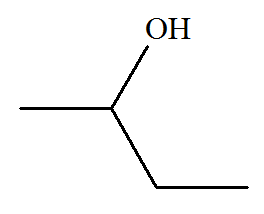
2)-
Formules spatiales des molécules.
- Convention :
- Un trait plein ––
représente une liaison entre deux atomes situés dans le plan de
la figure
- Un triangle allongé plein
![]() représente une liaison
entre un atome situé dans le plan de la figure et un atome situé
en avant de ce plan.
représente une liaison
entre un atome situé dans le plan de la figure et un atome situé
en avant de ce plan.
- Un trait hachuré
![]() ou un triangle hachuré
ou un triangle hachuré
![]() représente une liaison
entre un atome situé dans le plan de la figure et un atome situé
en arričre de ce plan.
représente une liaison
entre un atome situé dans le plan de la figure et un atome situé
en arričre de ce plan.
- Cas du carbone dans la molécule de méthane :
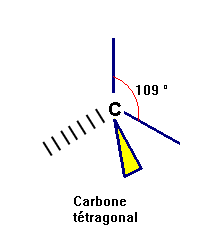 ou
ou
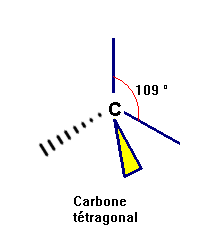
- Exercice :
La molécule de butan-2-ol :
- Représenter cette molécule en utilisant la représentation
de Cram et en considérant les groupes suivants : –
OH,
–H, –CH3 et
– C2H5.
- La représentation de
Cram permet de rendre compte de la
géométrie tétraédrique autour de l’atome de carbone.
III- Les différentes
relations de stéréoisomérie.
|
Stéréoisomčres : - Deux corps sont stéréoisomčres lorsqu'ils ont :
- Męme constitution (męme formule plane).
-
Mais des structures spatiales différentes
- Ils différent par l'agencement spatial de leurs atomes.
- On distingue :
- Les stéréoisomčres de conformation.
- Les stéréoisomčres de configuration.
|
b)-
Stéréoisomčres de conformation :
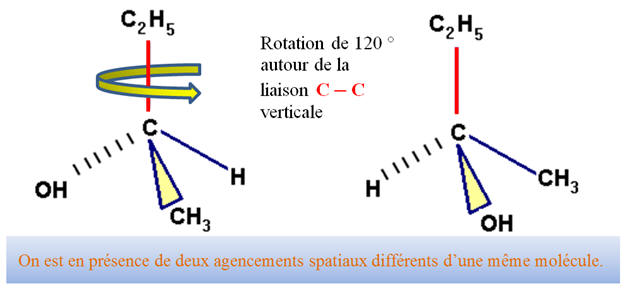
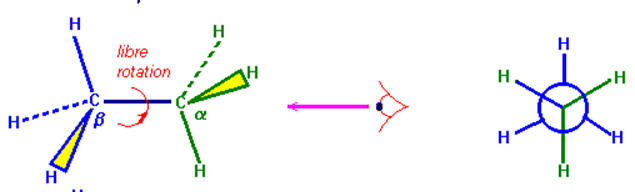
- On passe d’un stéréoisomčre de conformation ŕ un autre
par libre rotation autour d’une liaison simple.
- Exemple : libre rotation de 120 ° autour de la simple
liaison verticale
- On passe d’un stéréoisomčre de conformation ŕ un autre
par rotation autour de la simple liaison verticale
C – C.
- On est en présence de deux agencements spatiaux
différents d’une męme molécule.
c)-
Stéréoisomčres de configuration.
- Pour passer d’un stéréoisomčre de configuration ŕ un
autre, il faut briser des liaisons chimiques.
- Exemple :
- Stéréoisomčres obtenus aprčs avoir cassé puis reformé
deux liaisons chimiques.
- Deux stéréoisomčres de configuration sont deux
molécules différentes.
- Deux stéréoisomčres de conformation sont deux
agencements spatiaux d’une męme molécule.
2)-
Stéréoisomérie de configuration : Cas des composés ŕ un atome de
carbone asymétrique.
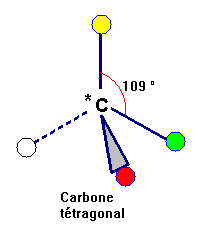
- C'est un atome de carbone tétragonal lié ŕ quatre atomes
ou groupes différents.
- On le repčre par un astérisque.
![]() Exercice
:
Exercice
:
- la molécule de butan-2-ol possčde-t-elle un
carbone asymétrique ? Si oui représenter les deux énantiomčres.
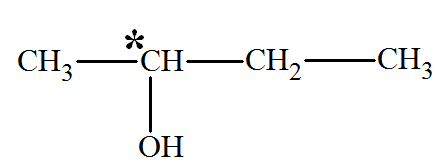

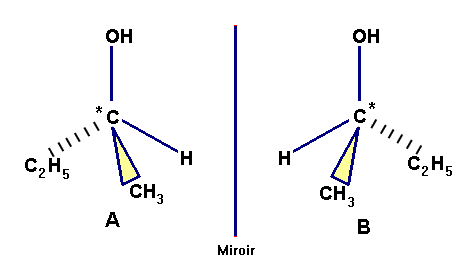
- La molécule
A n’est pas superposable ŕ son image
(la molécule B) dans un miroir.
- Une molécule possédant un seul atome de carbone
asymétrique est toujours chirale.
b)-
Énantiomérie et propriétés :
- Toute molécule possédant un atome de carbone asymétrique
peut exister sous deux configurations différentes, images l’une
de l’autre dans un miroir.
- Les stéréoisomčres correspondant sont appelés
énantiomčres.
- Énantiomčres :
stéréoisomčres de configuration qui sont image l'un de l'autre
dans un miroir.
- Énantiomérie :
relation existant entre deux stéréoisomčres de configuration
images l’un de l’autre dans un miroir.
- Mélange racémique :
- On appelle mélange racémique un mélange de quantités
égales de deux énantiomčres.
- Les énantiomčres présentent trčs souvent des propriétés
physiques et chimiques identiques.
- Par contre les propriétés biologiques et pharmacologiques
de deux énantiomčres sont presque toujours différentes.
-
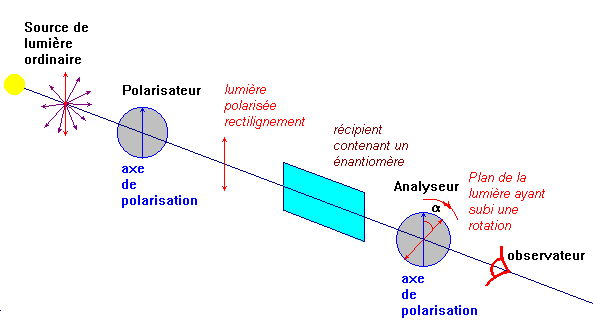
Deux énantiomčres n'ont pas le męme effet sur la lumičre
polarisé rectilignement.
- La solution d'une substance chirale peut faire tourner le plan de polarisation de la lumičre, on dit que cette substance est optiquement active.
- Elle possčde un pouvoir rotatoire.
- Une substance qui fait tourner le plan de polarisation de
la lumičre dans le sens des aiguilles d'une montre est dite
dextrogyre notée (+).
- Une substance qui fait tourner le plan de polarisation de
la lumičre dans le sens trigonométrique est dite lévogyre notée
(–).
- L'angle de rotation du plan de polarisation est appelé
pouvoir rotatoire.
- Deux énantiomčres ont des pouvoirs rotatoires opposés.
- Un mélange racémique ne possčde pas de pouvoir rotatoire.
3)-
Stéréoisomérie de configuration : Cas des composés ŕ deux atomes
de carbone asymétrique.
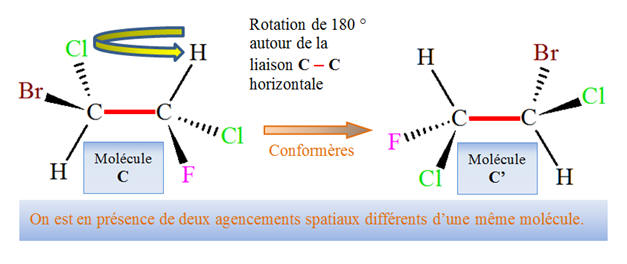
![]() La molécule de 1-bromo-1,2-dichloro-2-fluoroéthane
possčde 2 atomes de carbone asymétrique.
La molécule de 1-bromo-1,2-dichloro-2-fluoroéthane
possčde 2 atomes de carbone asymétrique.
![]() Chacun de ces
atomes de carbone asymétrique peut se trouver, indépendamment
de l’autre dans l’une des deux configurations possibles.
Chacun de ces
atomes de carbone asymétrique peut se trouver, indépendamment
de l’autre dans l’une des deux configurations possibles.
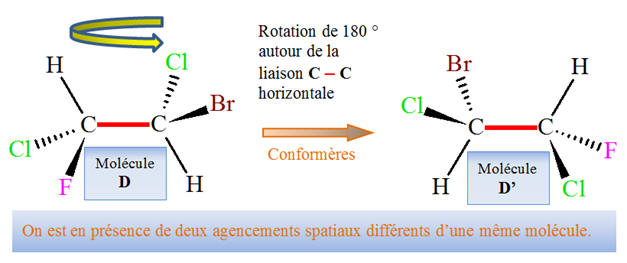
![]() Représenter
les deux configurations possibles et leurs énantiomčres.
Représenter
les deux configurations possibles et leurs énantiomčres.
- Formule développée de la molécule :
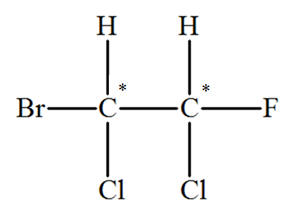
- Configurations possibles et énantiomčres :
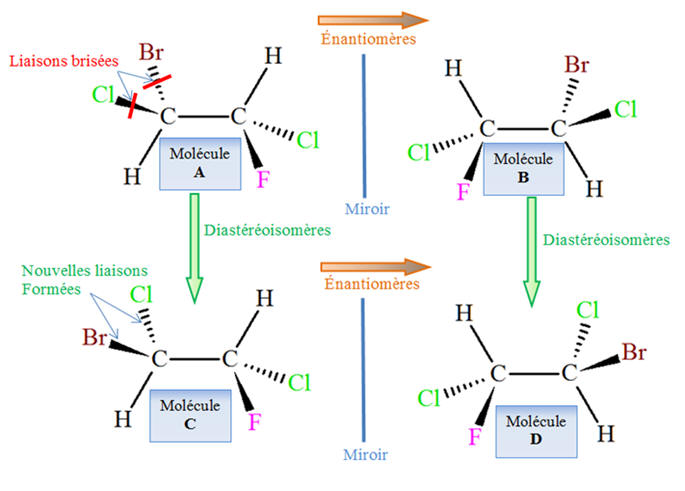
- Premier cas :
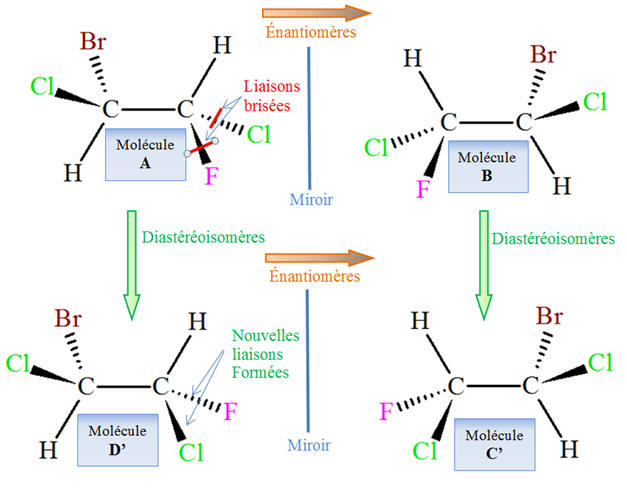
- Deuxičme cas :
- Remarque 1 :
- Remarque 2 :
- Les molécules
A et B sont images l’une de
l’autre dans un miroir : ce sont des énantiomčres.
- Les molécules
D et C sont images l’une de
l’autre dans un miroir : ce sont des énantiomčres.
- Les molécules
A et C sont des isomčres de
configuration non images l’un de l’autre dans un miroir : ce
sont des diastéréoisomčres.
- Les molécules
B et D sont des isomčres de
configuration non images l’un de l’autre dans un miroir : ce
sont des diastéréoisomčres.
- Les molécules
C et C’ sont des
stéréoisomčres de conformation : ce sont des conformčres (deux
agencements spatiaux d’une męme molécule).
- Les molécules
D et D’ sont des
stéréoisomčres de conformation : ce sont des conformčres (deux
agencements spatiaux d’une męme molécule).
- Les diastéréoisomčres sont des stéréoisomčres
de configuration qui ne sont pas énantiomčres.
- Les stéréoisomčres présentent des propriétés
physiques et chimiques différentes.
4)-
Stéréoisomérie de configuration : diastéréoisomčres Z / E.
►
Isomérie
Z et
E :
|
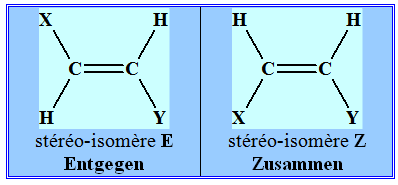
Isomérie Z et E : - Si, dans un alcčne de formule générale CHX = CHY, les deuxatomes d’hydrogčne sont dans le męme demi-plan par rapport ŕ l’axe de la double liaison C = C, le stéréo-isomčre est Z, dans le cas contraire, il est E. |
- Construire la molécule de but-2-čne.
- Donner la formule semi-développée et la formule
topologique des isomčres Z et E.
- Comment passe-t-on d'un isomčre ŕ l'autre ?
- Réponses :
|
|
|
|
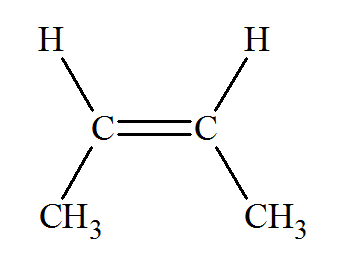
(E) but-2-čne Entgegen (en face, opposé), les hydrogčnes sont situés de part et d'autre
de la double liaison |
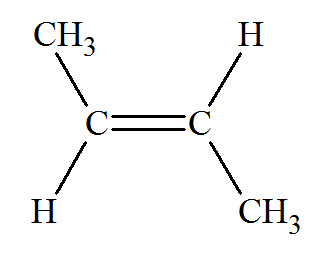
(Z) but-2-čne Zusammen (ensemble), les hydrogčnes sont situés du męme côté de la double
liaison. |
- Le (Z) but-2-čne et le (E) but-2-čne sont
des stéréoisomčres de configuration.
- Ce sont des corps purs distincts.
- Il n'y a pas libre rotation autour de la double liaison ŕ
température ambiante.
- Pour passer d'un stéréoisomčre ŕ l'autre, il faut briser
et reformer une liaison chimique.
- Deux isomčres
Z et E sont des
diastéréoisomčres.
-
Les isomčres Z et
E sont des corps purs
distincts que l'on peut isoler.
- Ils ont des propriétés physiques, chimiques, biologiques
différentes.
- La température d'ébullition normale du (Z)-but-2-čne
est de
5)-
Stéréoisomérie de conformation.
a)-
Conformations de l'éthane.
-
On appelle conformation d'une molécule les différentes
structures spatiales qu'elle peut prendre par suite de la
rotation autour de ses liaisons simples.
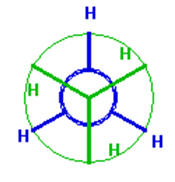
► Projection de
NEWMAN :
![]() Construire la molécule d'éthane. Noter α et
β chaque atome de carbone.
Construire la molécule d'éthane. Noter α et
β chaque atome de carbone.
![]() Regarder la molécule suivant
l'axe de la liaison carbone-carbone.
Regarder la molécule suivant
l'axe de la liaison carbone-carbone.
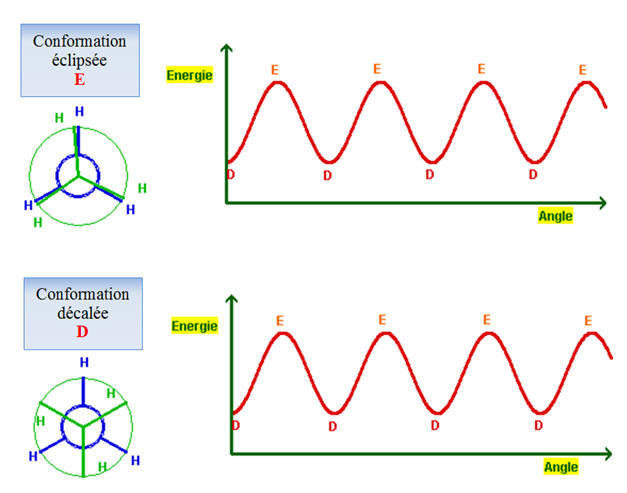
![]() Représenter les deux conformations remarquables (conformation
décalée et conformation éclipsée).
Représenter les deux conformations remarquables (conformation
décalée et conformation éclipsée).
- Réponses :
- Formule semi-développée de la molécule d'éthane :
- Le conformčre
E et le conformčre D sont des
stéréoisomčres de conformation.
- Ŕ température ambiante, il y a libre rotation autour de
la simple liaison.
- Le passage de l'un ŕ l'autre se fait sans rupture de
liaison.
► Aspect énergétique.
-
Laquelle des deux conformations est la plus stable ?
- Les conformations décalées sont plus stables que les
conformations éclipsées car les liaisons C ‑‑ H
sont les plus éloignées possibles dans les conformations
décalées.
- La conformation la plus stable d’une molécule est celle
pour laquelle les interactions répulsives entre les doublets de
liaisons et les interactions stériques dues ŕ l’encombrement des
gros substituants sont les plus faibles.
|
Les molécules A et B ont la męme formule brute, mais ne sont pas superposables |
||||
|
|
||||
|
A et B sont isomčres
de constitution |
NON
|
A et B ont-elles la męme formule
développée plane ? |
OUI
|
A et B sont
stéréoisomčres |
|
|
|
|||
|
A et B présentent-elles
la męme fonction chimique ? |
A et B peuvent-ils ętre interconvertis par des rotations autour
de liaisons simples ? |
||||||
|
|
|
|
|
||||
|
A et B sont isomčres
de fonction |
A et B sont isomčres de position
ou de chaîne
|
A et B sont isomčres
de configuration |
A et B sont isomčres
de conformation |
||||
|
|
|
||||||
|
A et B présentent-ils
le męme squelette carboné ? |
A et B sont-ils image
l'un de l'autre dans un miroir ? |
||||||
|
|
|
|
|
||||
|
A et
B sont isomčres
de chaîne |
A et B sont isomčres
de position |
A et B sont
diastéréoisomčres.
Exemple :
l'isomérie Z et E |
A et B sont
énantiomčres
Exemple : présence d'un carbone asymétrique,
molécule chirale. |
||||
2)-
Exercices :
a)- Exercice 7 page 270 : Reconnaître une molécule chirale.
b)- Exercice 8 page 270 : Utiliser la représentation
topologique.
c)- Exercice 10 page 270 : établir une représentation de
Cram.
d)- Exercice 15 page 271 : Représenter un couple
d’énantiomčres.
e)- Exercice 17 page 272 : de la formule semi-développée ŕ la
formule topologique.
f)- Exercice 20 page 272 : La vitamine
C.
g)- Exercice 22 page 273 : Autour des acides
α–aminés.
h)- Exercice 28 page 275 : Phéromone sexuelle de coléoptčre.
|
|