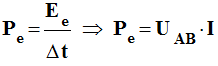|
QCM N° 03 Révisions Pour s'auto-évaluer |
Agir : défis du XXIe siècle |
|
|
|
|
QCM N° 03 Révisions :
Agir : défis du XXIe siècle.
Pour chaque question, indiquer
la (ou les) bonne(s) réponse(s). |
|||||
|
|
Énoncé |
A |
B |
C |
R |
|
1 |
L’air est constitué, en volume : |
d’environ 80 % de diazote, N2 et de 20 % de dioxygène, O2. |
d’environ 80 % de dioxygène, O2 et 20 % de diazote, N2 |
de 20 % de dioxygène, O2 et de 80 % de dioxyde de carbone, CO2. |
A |
|
2 |
Une combustion est : |
une transformation physique qui a lieu dans l’air. |
une transformation chimique nécessitant un comburant et un combustible. |
est une réaction chimique d’un combustible avec le dioxygène O2 (g). |
BC |
|
3 |
Lors d’une combustion complète du méthane :
|
du dioxygène est consommé. |
de l’eau et du dioxyde de carbone sont produits. |
le dioxyde de carbone est le seul produit. |
AB |
|
4 |
Une combustion incomplète d’un composé
organique :
|
peut produire du monoxyde de carbone, CO. |
ne produit que de l’eau ou du dioxyde de carbone. |
peut être dangereuse. |
AC |
|
5 |
Dans un circuit électrique, le courant continu circule : |
par convention de la borne positive vers la borne négative du générateur. |
par convention de la borne négative vers la borne positive du générateur. |
alternativement de la borne positive vers la borne négative et de la borne négative vers la borne positive. |
A |
|
6 |
Dans un circuit électrique parcouru par un
courant : |
les électrons se déplacent dans le sens conventionnel du courant. |
les électrons se déplacent dans le sens opposé de celui du courant. |
le courant circule de la borne + du générateur vers la borne –. |
BC |
|
7 |
Dans une solution, le courant électrique est un mouvement : |
d’électrons. |
d’ions. |
de protons. |
B |
|
8 |
L’intensité I du courant électrique : |
se mesure avec un ampèremètre. |
s’exprime en volt (V). |
se mesure avec un voltmètre. |
A |
|
9 |
Un voltmètre : |
se branche en série. |
se branche en dérivation. |
permet de mesurer une tension électrique. |
BC |
|
10 |
La loi d’Ohm s’écrit :
|
P = U . I |
I = R . U |
U = R . I |
C |
|
11 |
La puissance électrique reçue par un dipôle électrique : |
s’exprime en joule (J). |
dépend de la tension aux bornes du dipôle. |
dépend de la durée de fonctionnent du dipôle. |
B |
|
12 |
Une énergie peut s’exprimer en : |
watt. |
joule. |
kilowatt par heure. |
B |
|
13 |
Une pile utilise de l’énergie : |
électrique. |
mécanique. |
chimique. |
C |
|
14 |
Une solution aqueuse dans laquelle il y a plus d’ions H+ que d’ions HO–
est :
|
neutre. |
acide. |
basique. |
B |
|
15 |
Lors d’un chauffage à reflux, il n’y a pas de perte de matière grâce : |
au support élévateur. |
au chauffe-ballon. |
au réfrigérant. |
C |
|
Chimie |
|
►
L’air :
-
L’air est un mélange, constitué en volume, d’environ 80 % de diazote,
N2 et de 20 % de dioxygène,
O2.
►
La combustion :
-
Une combustion nécessite un combustible et un comburant (le plus
souvent le dioxygène de l’air).
-
Une combustion est une transformation chimique.
-
Exemple : combustion complète du butane :
2 C4H10
(g) + 13
O2
(g) →
8 CO2
(g) + 10
H2O
(g)
-
La réaction de combustion nécessite du dioxygène.
-
Elle produit du dioxyde de carbone et de la vapeur d’eau.
-
Lorsque l’apport en dioxygène est insuffisant, la combustion devient
incomplète et d’autres espèces chimiques peuvent se former : le
carbone C (fine poudre noire)
-
Ou le monoxyde de carbone
CO (gaz toxique).
-
Il convient alors d’écrire une équation chimique pour chaque espèce
carbonée formée.
-
Énergie libérée lors de la combustion : une combustion fournit de
l’énergie thermique.
-
Les énergies thermiques molaires sont de l’ordre de 103 à
104 kJ / mol.
►
Combustion complète du méthane :
-
Tableau d’avancement :
|
Équation |
CH4
(g) |
+ |
2 O2
(g) |
→ |
CO2 (g) |
+ |
2 H2O (g) |
|
État initial : |
n = |
|
n’
= |
|
0 |
|
0 |
|
État intermédiaire |
n – x |
|
n’
– 2 x |
|
x |
|
2 x |
|
État final |
n – xmax
= 0 |
|
n’ –
2 xmax
= 0 |
|
xmax |
|
2 xmax |
-
La réaction consomme du dioxygène.
-
Il se forme du dioxyde de carbone et de l’eau sous forme de vapeur.
►
Combustion incomplète :
-
Lorsque l’apport en dioxygène est insuffisant, la combustion devient
incomplète et d’autres espèces chimiques peuvent se former : le
carbone C (fine poudre noire)
-
Ou le monoxyde de carbone
CO (gaz toxique).
-
La combustion est incomplète d’un composé carboné peut s’avérer
dangereuse.
-
Il convient alors d’écrire une équation chimique pour chaque espèce
carbonée formée.
►
Le courant électrique continu :
-
Sens conventionnel du courant :
-
Dans un circuit, le courant sort par la borne positive du générateur
de courant.
-
En conséquence, le courant continu circule par convention de la borne
positive vers la borne négative du générateur.
-
Le sens conventionnel du courant est lié en sens de déplacement des
porteurs de charge positifs
-
Dans le circuit extérieur (fils, électrodes, ) les
porteurs de charge sont les électrons.
►
Courant dans les solutions :
-
Dans les solutions, les porteurs de charges sont les ions.
-
Les électrons ne se déplacent pas dans les solutions.
-
Le pont salin assure la migration des ions et empêche le mélange des
solutions, il est constitué d'une solution gélifiée de chlorure de
potassium.
-
Dans les solutions le courant électrique est dû à une double
migration des ions positif et négatif se déplaçant en sens inverse.
-
Les ions positifs se déplacent dans le sens conventionnel du courant
et les ions négatifs se déplacent dans le sens inverse (même sens que celui
des électrons).
►
Intensité du courant électrique :
-
L’intensité
I du courant électrique s’exprime en ampère,
symbole (A).
-
L’intensité I du courant électrique se mesure avec un ampèremètre.
-
L’ampèremètre se branche en série.
-
Schéma de l’ampèremètre :
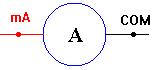
-
Branchement :
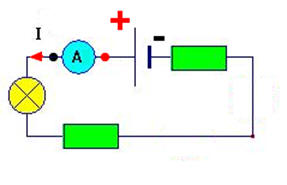
►
La tension électrique :
-
La tension électrique entre les deux points
A et
B d’un
circuit électrique se note : UAB.
-
La tension électrique entre deux points d’un circuit se mesure à
l’aide d’un voltmètre qui se branche en dérivation entre ces deux points.
-
La tension
UAB
s’exprime en volt de symbole V.
-
Schéma du voltmètre :
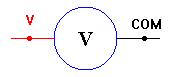
-
Branchement :
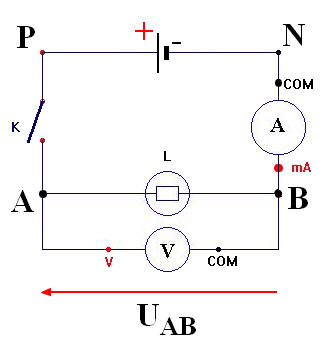
►
Loi d’ohm pour un conducteur ohmique :
|
U = R . I |
U :
Tension
aux bornes du conducteur ohmique (volt V) |
|
I :
Intensité du courant qui traverse le conducteur ohmique (ampère
A) |
|
|
R :
Résistance du conducteur ohmique (ohm Ω) |
-
Loi d’Ohm pour un conducteur ohmique de résistance
R :
-
Loi d'Ohm :
on
écrit : UAB = R.I
-
Schéma :
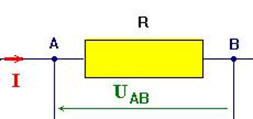
►
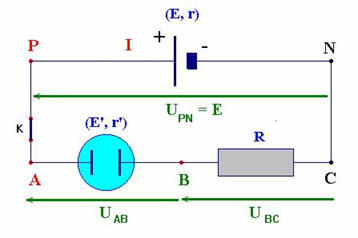
Puissance électrique reçue par un dipôle électrique :
-
La puissance électrique reçue par le récepteur est donnée par la
relation suivante :
|
|
|
I intensité en ampère A |
|
UAB tension en volt V
|
|
Pe puissance en watt W |
►
Énergie :
-
L’énergie
E consommée ou produite par un appareil de puissance
P est liée à sa durée de fonctionnement
Δt par la relation :
-
E =
P.Δt
-
Unités : l’énergie
E s’exprime en joule (J) et la puissance
P en watt (W).
-
Remarque :
-
Pour des raisons de commodité, la consommation électrique domestique
est donnée en kilowatt-heure (kW.h)
-
1 kW.h = 3,6
× 106
J
►
La pile :
-
Une pile est un appareil qui est capable de convertir de l'énergie
chimique Ech en énergie électrique
Ee.
-
Exemple :
|
Pile |
Énergie chimique Ech |
=> |
Énergie électrique Ee |
►
Solutions acides, neutres et basiques :
-
Une solution acide contient plus d'ions hydrogène
H+
(aq) que d'ions hydroxyde HO– (aq).
-
Une solution neutre contient autant d'ions hydrogène
H+
(aq) que d'ions hydroxyde HO– (aq).
-
Une solution basique contient moins d'ions hydrogène
H+
(aq) que d'ions hydroxyde HO– (aq).
►
Montage du chauffage à reflux :
|
Chauffage à Reflux
|
1- Réfrigérant. 2- Ballon. 3- Chauffe-ballon. 4- Sortie de l’eau. 5- Arrivée de l’eau. 6- Mélange réactionnel. 7- Vallet ou Support élévateur. |
|
Le
chauffage à reflux : Ce montage permet de maintenir le milieu réactionnel à une température constante, en l'occurrence pratiquement la température
d'ébullition du solvant. Les vapeurs
sont condensées dans le réfrigérant et retournent à l'état
liquide dans le ballon. Les réactifs
et les produits restent dans le milieu réactionnel. La présence du vallet est obligatoire. Elle permet d’enlever le chauffe-ballon
sans toucher au reste du montage (ballon et réfrigérant). Ainsi, on peut
rapidement refroidir le mélange réactionnel si un problème
survient et (ou) lorsque la réaction est terminée. Dans le réfrigérant, l’eau circule du bas vers le haut. Ainsi l’eau peut
remplir l’intérieur du réfrigérant. Il ne faut pas
fermer le réfrigérant pour éviter une augmentation de la
pression et travailler à la pression atmosphérique. |
|
|
|
|