|
QCM N° 02 Pour S'auto-évaluer Révisions |
Lois et modéles |
|
|
|
|
QCM N° 02 Révisions :
Pour chaque question,
indiquer la (ou les) bonne(s) réponse(s). |
|||||
|
N |
Énoncé |
A |
B |
C |
R |
|
La force gravitationnelle entre un corps A et un
corps
B : |
est
attractive |
est indépendante de la distance séparant ces
deux corps. |
a une valeur proportionnelle aux masses
des corps A et B. |
AC |
|
|
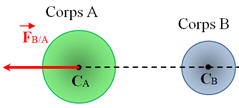
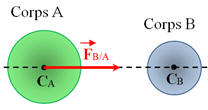
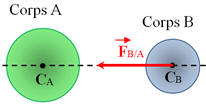
La représentation de la force gravitationnelle exercée par le corps B
sur le corps
A est :
|
|
|
|
B |
|
|
La valeur de la force gravitationnelle exercée par la Terre sur la
Lune est : |
supérieure à la valeur de la force exercée par la Lune sur
la Terre. |
inférieure à la valeur de la force exercée par la Lune
sur la Terre. |
égale à la valeur de la force exercée par la Lune
sur la Terre. |
C |
|
|
La valeur de la force gravitationnelle exercée par le Soleil sur la Terre
vaut : Données :
|
3,54 × 1028
N. |
3,54 × 1022
N. |
5,31 × 1031
N. |
B |
|
|
Le poids, sur la Terre, d’un corps de
masse
m :
|
est assimilable à la force d’attraction gravitationnelle exercée par la Terre sur
ce
corps. |
a une valeur s’exprimant
en kilogramme. |
est la même que le poids de ce corps
sur la Lune. |
A |
|
|
Le noyau d’un atome
est constitué : |
de protons et
d’électrons. |
de protons, de neutrons
et d’électrons. |
de protons
et de
neutrons. |
C |
|
|
L’atome de notation
symbolique
contient : |
26 protons
30 neutrons
26 électrons |
26 neutrons
56 nucléons
30 électrons |
30 neutrons
56 nucléons
26 protons |
AC |
|
|
Le changement d’état d’un corps pur, initialement liquide,
en gaz : |
se nomme
la sublimation. |
nécessite un apport
d’énergie. |
se produit à une température caractéristique
de ce corps pur. |
BC |
|
|
L’état liquide est
un état : |
compact et
désordonné. |
compact et
ordonné. |
dispersé et
désordonné. |
A |
|
|
Une solution de volume V = 100 mL contient 0,200 mol de saccharose. La concentration molaire
de cette solution vaut : |
2,00 × 10–3
mol / L |
0,500
mol / L |
2,00 mol / L |
C |
|
|
Lors d’une extraction
liquide / liquide : |
l’espèce chimique à extraire est plus soluble dans le solvant extracteur que dans le solvant
de départ. |
le solvant extracteur et le solvant de départ sont
non miscibles. |
l’espèce chimique extraite est moins soluble dans le solvant extracteur que dans le solvant
de départ. |
AB |
|
|
Un corps immobile dans
un référentiel d’étude : |
peut posséder de l’énergie
cinétique. |
peut posséder de l’énergie
de position. |
peut posséder de l’énergie
mécanique. |
BC |
|
|
L’énergie cinétique
d’un corps dépend : |
de sa
masse. |
de la valeur
de la
vitesse. |
du référentiel
d’étude. |
ABC |
|
|
L’énergie mécanique
s’exprime en : |
watt (W). |
newton (N). |
joule (J) |
C |
|
Les chapitres concernés
|
Physique |
|
Chimie |
►
L’interaction gravitationnelle :![]()
-
L’action exercée par un corps
B, de
masse m
B, situé au point
P,
-
Sur le corps
A, de masse
m A, situé au point
N,
-
Est modélise par une force
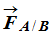
-
Schéma :
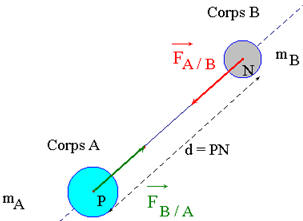
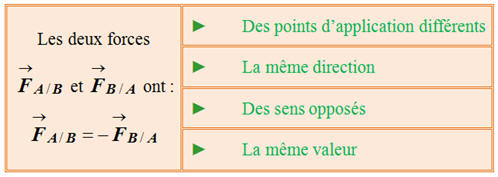
-
Les valeurs des
forces
![]() et
et
![]() sont :
sont :
-
Proportionnelles aux masses
-
Inversement proportionnelles aux carré de
leur distance.
-
Cette interaction est toujours attractive.
-
Elle agit entre particules ayant une masse.
-
Sa portée est infinie, mais sa valeur diminue
quand la distance augmente.
-
À l’échelle Astronomique, elle est
prédominante devant les autres interactions.
-
Elle explique la cohésion des édifices
astronomiques.
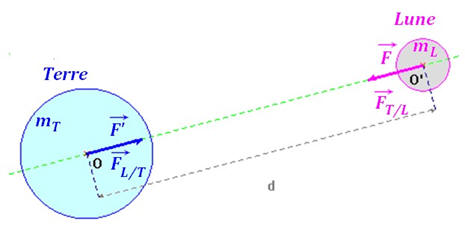
-
Dans le cas de l’interaction gravitationnelle
entre
-
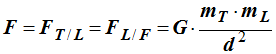
-
m
T : masse de la Terre :
m T
= 5,98
×
-
m
L : masse de la Lune :
m L
= 7,34
×
-
La valeur de la force gravitationnelle
exercée par la Terre sur la Lune est égale à la valeur de la force exercée
par la Lune sur la Terre.
►
Interaction Terre – Soleil :![]()
-
Masse de la Terre :
m T
= 5,98
×
-
Masse du Soleil :
m S
= 2,00
× 1030 kg.
-
Distance Terre – Soleil :
dS-T
= 1,50
× 108 km
-
G ≈
6,67
× 10
– 11
m
2. kg–
2. N
-
Valeur de
F =
FT / S.
-
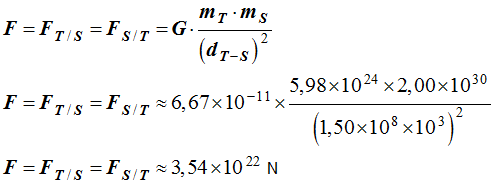
►
Poids et force gravitationnelle :
![]()
-
Tout corps
A, de centre
C et de
masse m,
placé au voisinage de la Terre subit une attraction.
-
Le centre de la Terre est noté
T, sa
masse m T
et son rayon
R T.
-
Schéma :
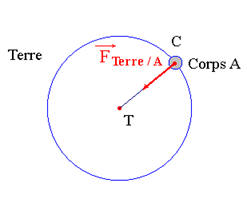
-
L’attraction exercé par la Terre sur le corps
A est modélisée par la force
![]() .
.
-
Sur la terre, tout corps de masse
m
est soumis à une force appelée poids du corps :
-
Expression du poids :
P =
m.g.
-
P
poids en Newton N, m la
masse en kg et g le facteur d’attraction terrestre :
g = 9,8 N
/ kg.
-
Le poids d’un objet sur Terre est
pratiquement égal à la force gravitationnelle exercée par la Terre sur
l’objet.
-
Remarque :
-
La différence entre le poids d’un objet sur
la Terre et la force de gravitation exercée par la Terre sur l’objet
provient de la rotation de la Terre sur elle-même.
-
Le poids d’un corps peut s’identifier à la
force gravitationnelle exercée par la Terre sur l’objet.
-
La valeur du poids varie en fonction de la
latitude et de l’altitude.
-
Un corps de masse
m n’a pas le même poids sur
-
Un objet de masse
m est environ six fois plus
léger sur la Lune que sur la Terre.
-
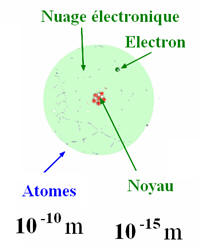
Un atome est constitué :
-
D’un noyau contenant
A nucléons :
Z
protons et (A – Z) neutrons.
-
D’un nuage électronique constitué de
Z
électrons.
-
Le nombre de nucléons est noté
A, on
l’appelle aussi le nombre de masse.
-
Le nombre de protons que contient le noyau
est noté Z, on l’appelle aussi le numéro atomique ou le nombre de
charge.
►
Symbole du noyau d’un atome.![]()
-
Les deux grandeurs
A et
Z
suffisent pour caractériser un noyau ou un atome.
-
Le symbole du noyau s’obtient à partir du
symbole de l’atome correspondant.
-
Un atome de symbole
X qui a pour
nombre de masse A et pour nombre de charge
Z est représenté
symboliquement par
![]() :
:
-
Exemple : symbole du noyau de l’atome de fer
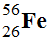 .
.
-
Le noyau de l’atome de fer est constitué
de :
-
Z
= 26 protons,
-
A – Z = 30 neutrons.
-
Cet atome possède un cortège électronique
constitué de :
-
Z = 26 électrons.
-
Un atome comprend :
Z protons,
Z
électrons, et A – Z neutrons.
►
Changement d’état physique :![]()
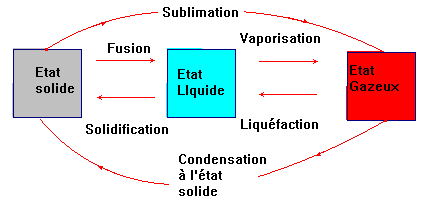
-
L’énergie thermique apportée à un corps pur
moléculaire peut :
-
Provoquer une augmentation de la température
avec rupture des interactions intermoléculaires et accroissement de
l’agitation des molécules
-
Provoquer un changement d’état physique avec
seulement rupture d’interaction intermoléculaires, la température restant
constante.
-
Le changement d’état d’un corps pur,
initialement liquide, en gaz nécessite un apport d’énergie.
-
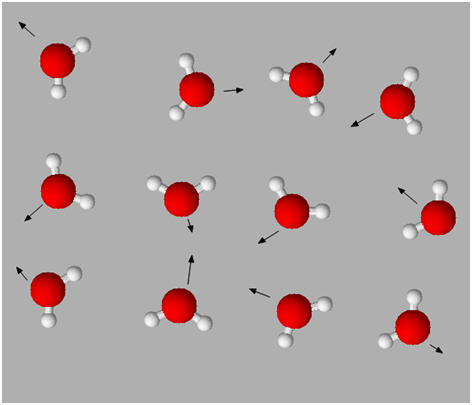
L’état gazeux :
-
L’état gazeux est un état dispersé et
désordonné.
-
Les molécules et les ions sont éloignés les
uns des autres et se déplacent dans toutes les directions de façon
désordonnée.
-
Les interactions entre les entités chimiques
sont faibles.
-
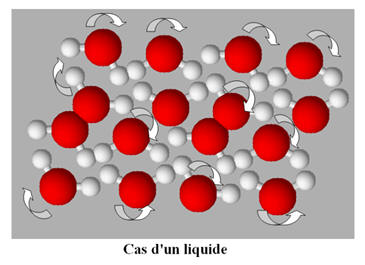
L’état liquide :
-
L’état liquide est un état condensé et
désordonné.
-
À l’état liquide, les entités chimiques sont
les unes contre les autres et peuvent glisser les unes sur les autres.
-
Les entités chimiques sont en mouvement
constant.
-
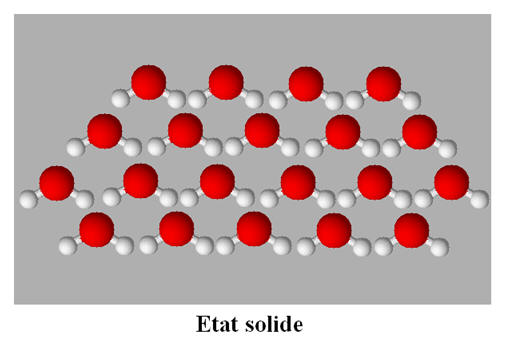
L’état solide :
-
L’état solide est un état condensé et
ordonné.
-
Les particules dans la matière condensée sont
soumises à des interactions attractives qui les maintiennent en contact les
unes avec les autres, tandis que les interactions répulsives leur imposent
des structures d’empilement.
►
Concentration molaire volumique :![]()
-
La concentration molaire volumique
C
(s) en soluté apporté est égale au
quotient de la quantité de matière n
(s) en soluté apporté par le volume V de la solution :
-
Application numérique :
-
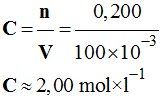
►
Extraction liquide / liquide.![]()
-
Lors d’une extraction liquide/liquide :
-
L’espèce chimique à extraire est plus soluble
dans le solvant extracteur que dans le solvant de départ.
-
Et le solvant extracteur et le solvant de
départ sont non miscibles.
-
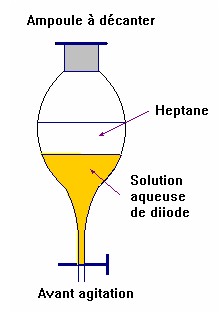
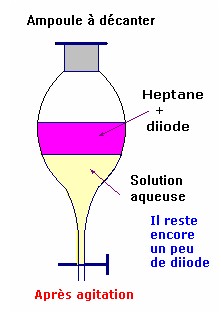
L’extraction par un solvant se réalise dans
une ampoule à décanter.
-
Le choix du solvant dépend de l’espèce
chimique recherchée.
-
Exemple :
extraction du diiode présent
dans une solution par l’heptane.
|
|
|
|
|
|
-
Énergie cinétique :
-
L’énergie cinétique
EC
d’un solide en mouvement de translation est égale au demi-produit de la
masse m du solide par le carré de la vitesse
v2
du solide.
-
On écrit :
-
![]()
-
Unités :
|
EC
en joule (J) |
|
m
en kilogramme (kg) |
|
v
en mètre / seconde (m / s) |
-
L’énergie cinétique caractérise un solide en
mouvement.
-
Elle est :
-
Proportionnelle à la masse
m du solide
-
Proportionnelle au carré de la vitesse
v
du solide.
-
Elle dépend du référentiel d’étude.
-
C’est une grandeur supérieure ou égale à
zéro.
-
Si le système est immobile dans un
référentiel, l’énergie cinétique est nulle dans ce référentiel.
-
Énergie potentielle de pesanteur :
-
L’énergie potentielle de pesanteur
Ep
d’un solide est l’énergie qu’il possède du fait de sa position par rapport à
la Terre, c’est-à-dire du fait de son altitude.
-
Un solide de masse
m est soumis à son
poids
![]() sur la Terre.
sur la Terre.
-
L’énergie
potentielle de pesanteur d’un solide est l’énergie qu’il possède du fait de
son interaction avec la Terre. La valeur de cette énergie dépend de la
position du solide par rapport à la Terre.
-
Expression :
Ep =
m .
g .
z.
|
Ep = m . g . z. |
m :
masse de l’objet en kilogramme kg. |
|
g :
facteur d’attraction terrestre :
g
= 9,81 N / kg ou
g
= |
|
|
z :
altitude du centre d’inertie de l’objet en mètre m. |
|
|
Ep : énerie potentielle de pesanteur en joule J |
-
L’énergie potentielle est définie à une
constante additive près.
-
La différence d’énergie potentielle ne dépend
pas du choix de l’origine.
-
Énergie mécanique d’un solide :
-
L’énergie mécanique d’un solide est la somme
de son énergie cinétique et de son énergie potentielle.
-
Relation :
-
Em
= EC +
EP.
-
Unité : joule (J)
-
L’énergie cinétique
EC
d’un solide en mouvement de translation est égale au demi-produit de la
masse m du solide par le carré de la vitesse
v2
du solide.
-
On écrit :
-
![]()
-
Unités :
|
EC
en joule (J) |
|
m
en kilogramme (kg) |
|
v
en mètre / seconde (m / s) |
-
L’énergie cinétique caractérise un solide en
mouvement.
-
Elle est :
-
Proportionnelle à la masse
m du solide
-
Proportionnelle au carré de la vitesse
v
du solide.
-
Elle dépend du référentiel d’étude.
-
C’est une grandeur supérieure ou égale à
zéro.
►
Énergie mécanique d’un solide :![]()
-
L’énergie mécanique d’un solide est la somme
de son énergie cinétique et de son énergie potentielle.
-
Relation :
-
Em
= EC +
EP.
-
Unité : joule (J)
|
|
|
|