|
Pour s'auto-évaluer |
Atomes et Molécules. |
|
QCM N° 06 :
Atomes et Molécules.
Pour chaque
question, indiquer la (ou les) bonne(s) réponse(s). Énoncé A B C R 1 Les gaz nobles : Sont quasiment inerte chimiquement Possèdent tous un
octet électronique Ont leur couche
externe saturée AC 2 Combien de liaisons covalentes l’atome de carbone
C (Z = 6) forme-t-il ? 6 4 2 B 3 L’atome d’hydrogène
H et l’atome d’oxygène O
ont pour numéros atomiques respectifs 1 et 8. La molécule d’eau H2O
a pour représentation de Lewis :
C 4 L’atome de carbone
C et l’atome d’oxygène O
ont pour numéros atomiques respectifs 6 et 8. La
molécule de dioxyde de carbone
CO2
a pour représentation de Lewis :
B 5 L’atome d’azote
N a pour
numéro atomique
Z = 7. La molécule de diazote
N2
a pour formule de Lewis :
A 6 Dans la molécule de méthanal, les
atomes de carbone (Z
= 6) et d’oxygène (Z
= 8) : Mettent en commun 2
électrons Mettent en commun 4
électrons Respectent la règle
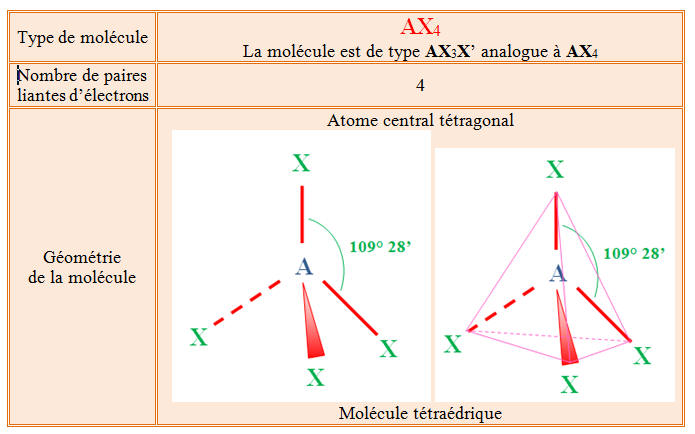
de l’octet BC 7 La molécule de
fluorométhane est :
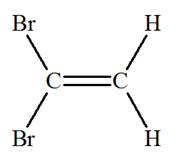
plane Triangulaire pyramidale C 8 La molécule de chloramine est : plane Triangulaire pyramidale C 9 La molécule de 1,1 – dibromoéthène
représentée ci-dessous : Est celle de
l’isomère Z Est celle de
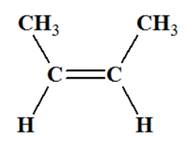
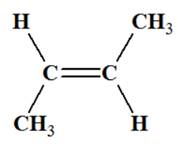
l’isomère E Ne présente pas d’isomérie Z / E. C 10 La molécule de but-2-ène
représentée ci-dessous :
Est celle de
l’isomère Z Est celle de
l’isomère E Ne présente pas d’isomérie Z / E. B 11 L’atome d’oxygène (Z = 8)
possède : 6 électrons de valence 8 électrons de valence 2 électrons de valence A 12 L’atome d’oxygène forme :
4 liaisons covalentes 2 liaisons covalentes 8 liaisons covalentes B 13 La formule de Lewis d’une molécule
est la représentation : Des liaisons entre les
atomes Des atomes de la
molécule et de leurs électrons de valence regroupés en
doublets Des doublets liants de
la molécule B 14 Dans la molécule de méthane
CH4,
l’atome de carbone est au : Centre d’un carré dont
les atomes d’hydrogène sont aux sommets Sommet d’une pyramide
dont les atomes d’hydrogène sont les sommets Centre d’un tétraèdre
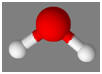
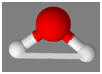
dont les atomes d’hydrogène sont les sommets C 15 La représentation dans l’espace de la
molécule d’eau est : A 16 On considère la molécule de formule
semi-développée :
CH3–CH=CH–CH3. Cette formule :
Représente
deux
isomères
Z / E
Représente
quatre
isomères
Z / E
Ne représente
pas
d’isomérie
Z / E A
►
Les gaz nobles. -
Les gaz rares ou nobles sont
chimiquement très stables. - Alors que les autres atomes peuvent
participer à des réactions chimiques, former des ions, les gaz
nobles ou rares, ne sont pas impliqués dans de telles
transformations chimiques. -
Cette stabilité est liée au fait
que leur dernière couche électronique (couche électronique
externe) est saturée (pleine). -
Exemple : la couche électronique
externe de l’hélium He contient 2 électrons (couche
K
qui est saturée à 2 électrons. - Les autres gaz rares possèdent 8
électrons sur leur couche électronique externe. -
On parle de structure en
DUET :
atome ou ion qui possède 2 électrons sur sa couche électronique
externe (K). -
Et de structure en
OCTET : atome ou ion qui possède 8 électrons sur sa
couche électronique externe.
►
Règles du
DUET et de OCTET :
-
Au cours des transformations
chimiques, les atomes tendent à acquérir la structure
électronique du gaz rare de numéro atomique le plus proche : -
Soit 2 électrons sur la couche
électronique externe lorsque ce gaz rare est Hélium c’est la
règle du DUET. -
Soit 8 électrons sur la couche
électroniques externe, c’est la règle de l’OCTET. -
Ils acquièrent de ce fait une
stabilité maximale.
►
Molécules :
-
Une molécule est une entité
chimique électriquement neutre Elle est formée d’un nombre
limité d’atomes liés entre eux par des liaisons de covalence. -
Le nombre d’atomes d’une molécule
est son atomicité. -
Dans la formule d’une molécule,
les symboles des éléments présents dans la molécule sont écrits
côte à côte avec, en indice, en bas à droite, le nombre d’atomes
de chaque élément. -
L’indice 1 n’est jamais spécifié. -
La nature et le nombre des atomes
présents dans une molécule sont donnés par sa formule brute.
►
La liaison
covalente. -
Lorsqu’ils forment des molécules,
les atomes mettent en commun certains des électrons de leurs
couches électroniques externes de façon à s’entourer de 2 ou 8
électrons. -
En conséquence, dans une
molécule, les atomes sont liés par des liaisons covalentes ou
des liaisons de covalence. -
La liaison covalente consiste à
la mise en commun par deux atomes d’un ou plusieurs doublets
d’électrons appelés doublets de liaison ou doublets liants. -
Remarque : les électrons mis en
commun appartiennent à chacun des deux atomes et doivent être
pris en compte dans le total des électrons de chaque atome. -
En formant des liaisons de
covalence, chaque atome acquiert, en général, une structure
électronique en
octet ou en
DUET,
semblable à celle du gaz noble qui le suit dans la
classification périodique. -
Le nombre de liaisons covalentes
qu’établit un atome est généralement égal au nombre d’électrons
qui lui manque pour acquérir une structure électronique en
OCTET ou
DUET.
►
Nombre de
liaisons covalentes l’atome de carbone C : -
Pour l’atome de carbone,
Z = 6 -
Configuration électronique :
K2L4 -
La liaison covalente consiste à
la mise en commun par deux atomes d’un ou plusieurs doublets
d’électrons appelés doublets de liaison ou doublets liants. -
Le nombre de liaisons covalentes
qu’établit un atome est généralement égal au nombre d’électrons
qui lui manque pour acquérir une structure électronique en
OCTET ou
DUET. -
En conséquence, l’atome de
carbone peut mettre en commun les 4 électrons (règle de
l’Octet : 4 + 4) de la couche
L. -
Il peut former 4 liaisons
covalentes.
►
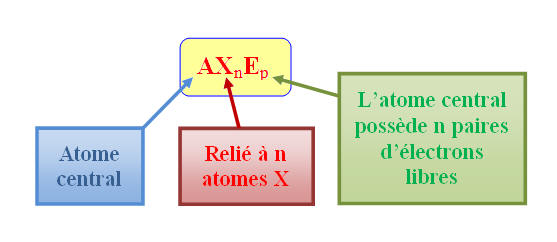
Méthode VSEPR pour la géométrie
des molécules.
►
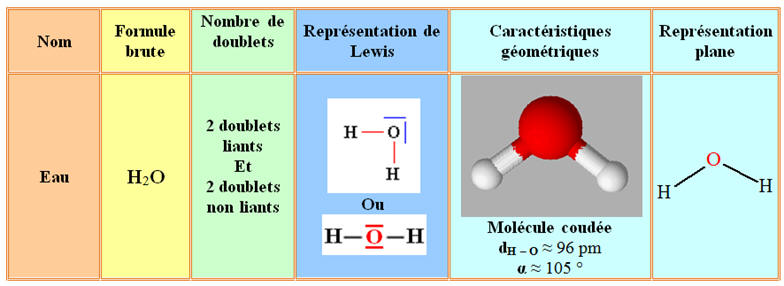
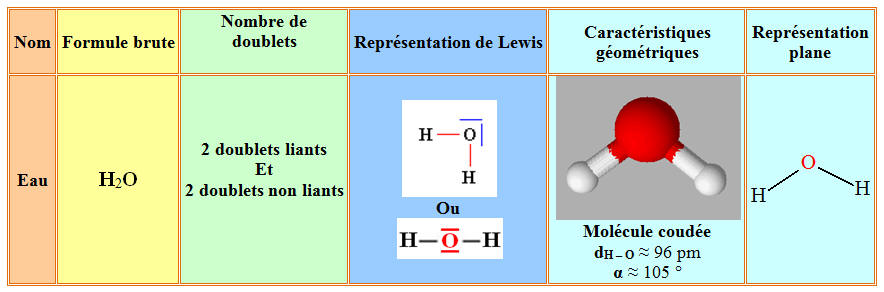
La molécule d’eau :
►
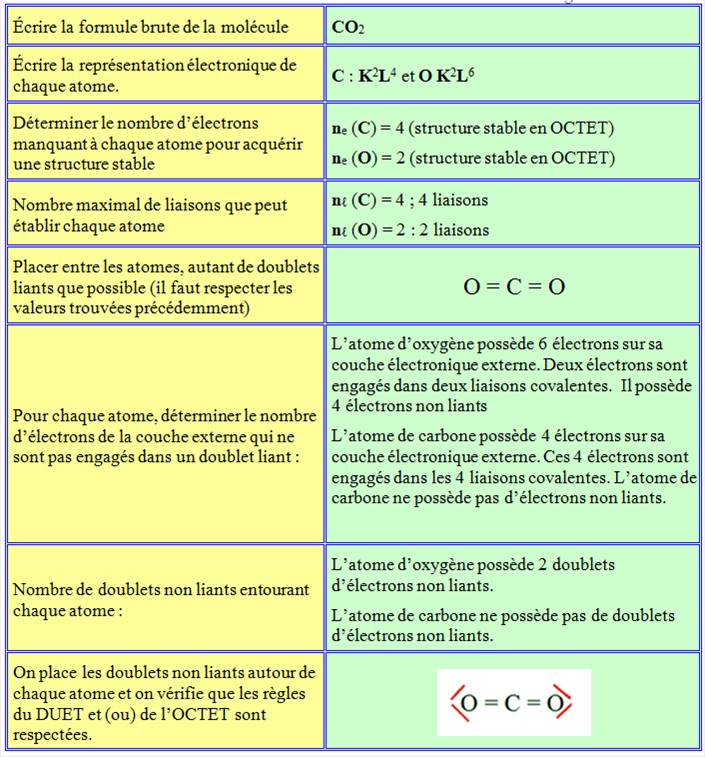
La molécule de
dioxyde de carbone CO2 :
►
Molécule de
diazote N2 : -
Pour l’atome d’azote, Z =
7 -
Configuration électronique :
K2L5 -
La liaison covalente consiste à
la mise en commun par deux atomes d’un ou plusieurs doublets
d’électrons appelés doublets de liaison ou doublets liants. -
Le nombre de liaisons covalentes
qu’établit un atome est généralement égal au nombre d’électrons
qui lui manque pour acquérir une structure électronique en
OCTET ou
DUET. -
En conséquence, l’azote peut
mettre en commun les 3 (Règle de l’Octet : 5 + 3) électrons de
la couche
L. -
Chaque atome d’azote, de la
molécule de diazote
possède 3 doublets liants et un doublet non liant.
►
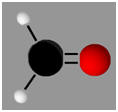
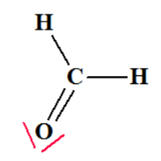
La molécule de
méthanal :
-
Les atomes de carbone et
d’oxygène mettent en commun 4 électrons et respectent la règle
de l’Octet.
-
Chaque atome d’hydrogène respecte
la règle du Duet.
►
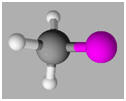
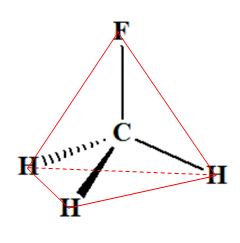
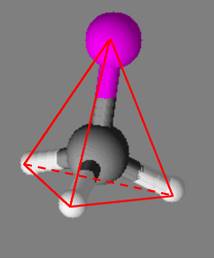
Molécule de
fluorométhane : -
La molécule de fluorométhane est
pyramidale.
CH3F
- Représentation schématique :
►
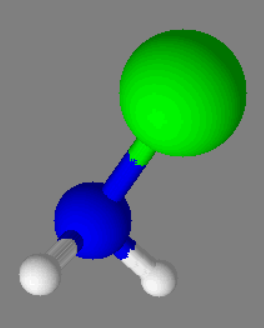
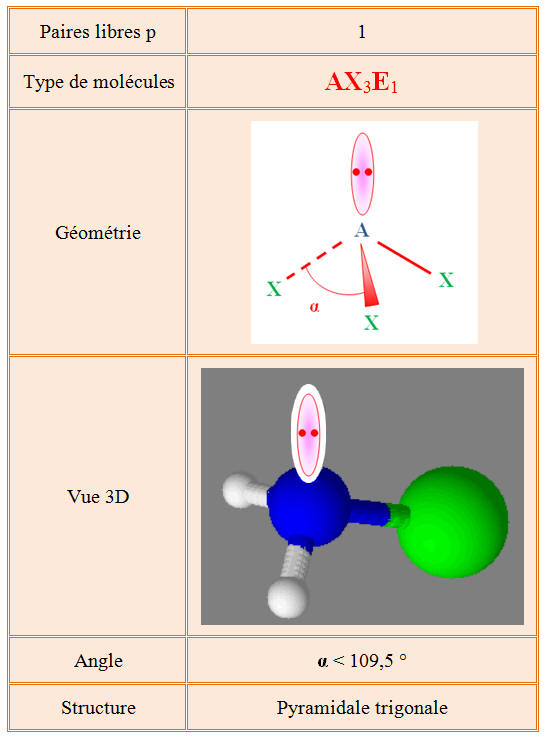
Molécule de chloramine : -
C’est une molécule pyramidale.
►
Isomérie :
Définition. -
Deux molécules isomères ont même
formule brute mais des enchaînements d’atomes différents. -
Les isomères ont des propriétés
physiques et chimiques différentes et constituent des espèces
chimiques distinctes.
►
Formule brute. -
La formule brute d’une molécule
indique la nature et le nombre des atomes constituant la
molécule. -
Elle ne donne aucune indication
sur la structure de la molécule : chaîne carbonée, groupe
fonctionnel,…
►
La formule développée plane. -
Elle indique l’enchaînement des
atomes et la nature des liaisons qui les unissent.
►
Formule
semi-développée. -
Elle dérive de la formule
développée. - Elle ne fait pas apparaître les liaisons entre un
atome d’hydrogène et un autre atome.
►
Formule
topologique. -
La chaîne carbonée est
représentée sous forme de ligne brisée. - Les atomes autres que de
carbone
C et d’hydrogène
H sont représentés de
manière explicite ainsi que les atomes d’hydrogène
H
qu’ils portent.
►
Les isomères de
constitution : -
Les isomères de constitution sont
des molécules qui ont la même formule brute mais qui différent
par l’enchaînement de leurs atomes. -
Parmi les isomères de
constitution, on distingue : -
Les isomères de chaîne : les
chaînes carbonées sont différentes. -
Les isomères de position : la
position du groupe fonctionnel ou de la double liaison sont
différentes. -
Les isomères de fonction : les
groupes fonctionnels sont différents.
►
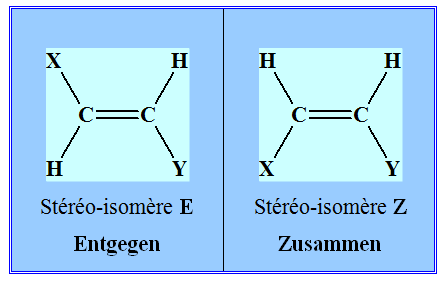
L’isomérie Z et E ou stéréo-isomérie. -
Si, dans un alcène de formule
générale
CHX=CHY, les deux atomes d’hydrogène sont dans
le même demi-plan par rapport à l’axe de la double liaison
C=C, le stéréo-isomère est
Z, dans le cas contraire,
il est E.
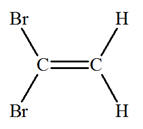
-
La molécule de 1,1 – dibromoéthène,
représentée ci-dessous, ne présente pas d’isomérie
Z /
E.
-
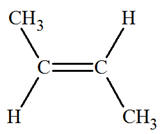
La molécule de but-2-ène, représentée
ci-dessous, est celle de l’isomère
E.
-
La molécule de formule
semi-développée,
CH3–CH=CH–CH3,
représente deux isomères Z /
E.
►
L’atome d’oxygène :
-
L’atome d’oxygène possède 6 électrons
sur sa couche électronique externe, il possède 6 électrons de
valence. -
Il manque deux électrons 2 électrons
à sa couche électronique externe pour acquérir une structure stable
(Octet). -
L’atome d’oxygène forme 2 liaisons
covalentes.
►
Représentation de
LEWIS. -
La représentation de
LEWIS
précise l’enchaînement des atomes et la position des doublets liants
et non liants. -
Dans la représentation de
LEWIS
d’une molécule : -
Le symbole de l’élément représente le
noyau de l’atome et les électrons internes, -
Chaque doublet d’électrons externes
est figuré par un tiret. -
On distingue les doublets liants et
les doublets non liants : -
Un doublet liant est représenté par
un tiret entre les symboles de deux atomes, -
Un doublet non liant est représenté
par un tiret situé autour du symbole d’un atome auquel il
appartient.
►
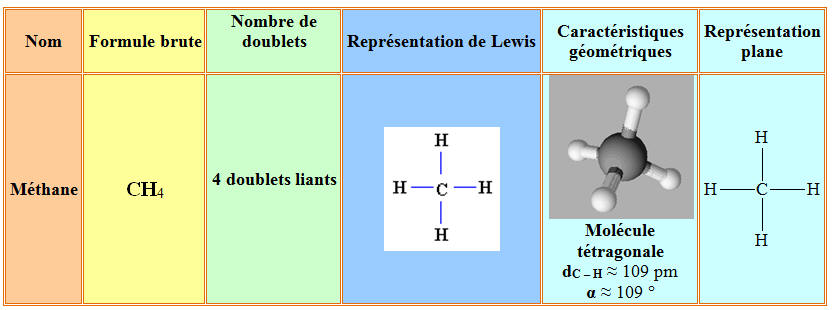
Molécule de
méthane : -
Dans la molécule de méthane
CH4,
l’atome de carbone est au centre d’un tétraèdre dont les atomes
d’hydrogène sont les sommets.
►
La molécule d’eau :
►
Isomérie Z / E :
(voir au-dessus)
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
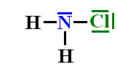
![]()

 ou
ou
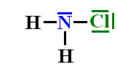
 et
et