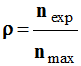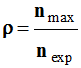|
QCM N° 19 a Pour s'auto-évaluer |
Synthèses organiques |
|
|
||
|
|
|
QCM N° 19 a : Synthèse Organiques.
Pour chaque question,
indiquer la (ou les) bonne(s) réponse(s). |
|||||
|
|
Énoncé |
A |
B |
C |
R |
|
1 |
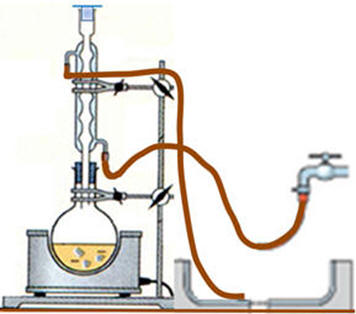
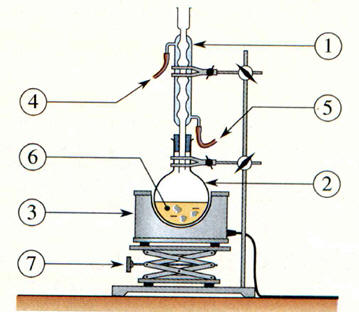
Le montage de chauffage à reflux schématisé ci-dessous est incorrect car : |
le réfrigérant ne doit pas
être bouché. |
il manque le support
élévateur. |
l’eau doit arriver par le haut du
réfrigérant. |
A
B |
|
2 |
Le
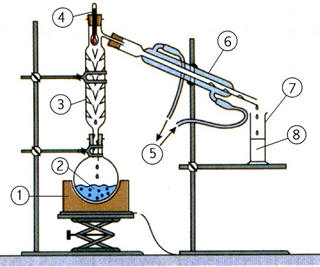
montage schématisé ci-dessous : |
est un montage de distillation
fractionnée. |
est un montage
d’hydrodistillation. |
permet de séparer des espèces liquides
miscibles. |
A
C |
|
3 |
Lors de l’étape de chauffage à reflux, le réfrigérant est nécessaire
pour : |
éviter les pertes de matière
par évaporation. |
recueillir les
produits
formés. |
liquéfier les espèces
vaporisées. |
A B
C |
|
4 |
Pour isoler un produit liquide du reste du mélange réactionnel, on
peut effectuer : |
une extraction
liquide /
liquide. |
une distillation. |
une mesure de température
de fusion. |
A
B |
|
5 |
Pour identifier un produit solide obtenu lors d’une synthèse, on peut
effectuer : |
une chromatographie
sur
couche mince. |
une mesure de la température
d’ébullition. |
une mesure de la température
de fusion. |
A
C |
|
6 |
Pour déterminer le rendement d’une synthèse, il faut connaître : |
le réactif
limitant. |
la quantité de produit
formé. |
la quantité maximale de produit qui
peut être formé. |
A B
C |
|
7 |
Lors d’une synthèse, il se forme 0,42 mol d’un produit alors qu’au maximum 0,60 mol de ce produit est attendu. Le rendement de la synthèse est : |
0,60 mol |
0,42 |
0,70 |
C |
|
8 |
Le rendement de la synthèse d’une espèce chimique est égal à 90 %. La quantité maximale attendue de cette espèce est 0,20 mol. La quantité de produit obtenu expérimentalement est : |
0,20 mol |
0,22 mol |
0,18 mol |
C |
|
9 |
Les
nano-objets ont une taille : |
comprise entre
10–3
et 10–5 m. |
comprise entre
10–10
et 10–7 m. |
qui leur confère des propriétés
particulières. |
B
C |
|
10 |
Si nexp est la quantité de produit obtenu et nmax la quantité maximale attendue, le rendement d’une synthèse vaut : |
|
|
|
B |
Essentiel :
►
Montage du chauffage à reflux ;
|
Chauffage à Reflux |
1- Réfrigérant. 2- Ballon. 3- Chauffe-ballon. 4- Sortie de l’eau. 5- Arrivée de l’eau. 6- Mélange réactionnel. 7- Vallet ou
Support
élévateur. |
|
Le chauffage à reflux : Ce montage permet de maintenir le milieu réactionnel à une température constante, en l'occurrence pratiquement la température d'ébullition du
solvant. Les vapeurs sont condensées dans le réfrigérant et retournent à l'état liquide
dans le ballon. Les réactifs et les produits restent dans le milieu réactionnel. La présence du vallet est obligatoire. Elle permet d’enlever le chauffe-ballon sans toucher au reste du montage (ballon et réfrigérant). Ainsi, on peut rapidement refroidir le mélange réactionnel si un problème survient et (ou) lorsque la réaction est terminée. Dans le réfrigérant, l’eau circule du bas vers le haut. Ainsi l’eau peut
remplir l’intérieur du réfrigérant. Il ne faut pas fermer le réfrigérant pour éviter une augmentation de la pression et travailler à la pression atmosphérique. |
►
Distillation fractionnée :
|
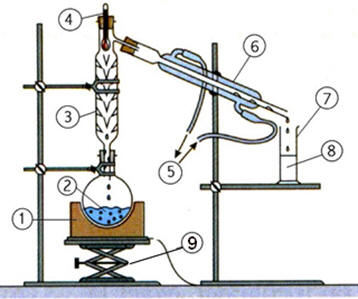
(1)‑Chauffe-ballon. (2)‑Mélange. (3)‑Colonne de Vigreux. (4)‑Thermomètre. (5)‑Arrivée et Sortie de l’eau. (6)‑Condenseur. (7)‑Éprouvette. (8)‑Distillat. (9)- Vallet ou Support élévateur |
-
Le mélange à distiller est placé dans un
ballon surmonté d’une colonne à distiller : colonne de Vigreux.
- On chauffe le ballon jusqu’à ébullition du mélange.
- Les vapeurs des différentes espèces chimiques montent dans la
colonne à distiller.
-
La distillation fractionnée permet de séparer
et de recueillir les constituants d’un mélange d’espèces chimiques ayant des
températures d’ébullition différentes.
-
L’espèce chimique extraite en premier est
l’espèce la plus volatile, celle dont la température d’ébullition est la
plus faible.
►
Hydrodistillation :
L’entraînement à la vapeur ou hydrodistillation ou distillation simple.
-
L’hydrodistillation permet d’extraire des
espèces chimiques volatiles, très peu solubles dans l’eau, présentes dans
les fleurs, les écorces, les fruits, etc. et d’obtenir des huiles
essentielles.
|
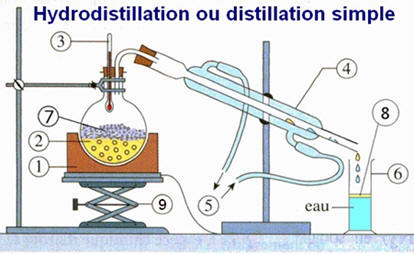
Distillation de la lavande |
1 :
Chauffe-ballon
2 :
Mélange (Eau-fleurs de lavande)
3 :
Thermomètre
4 :
Réfrigérant à eau
5 :
Arrivée et Sortie de l’eau
6 :
Éprouvette 7 :
Fleurs de lavande. 8 :
Huile essentielle de lavande
9 :
Vallet ou Support élévateur |
-
Dans l’entraînement à la vapeur, l’ébullition
du mélange d’eau et du produit crée un courant de vapeurs.
-
Ce courant de vapeurs est constitué de
vapeurs d’eau et de vapeurs des huiles essentielles du produit.
-
On condense ce mélange gazeux pour obtenir un
distillat.
-
Ce
distillat est constitué d’eau à l’état liquide et des huiles essentielles à
l’état liquide.
-
Les
huiles essentielles étant peu miscibles avec l’eau et moins dense que l’eau,
elles surnagent.
-
Exemple :
on extrait par entraînement à la vapeur, l’huile essentielle des fleurs de
lavande.
-
Cette huile essentielle est un mélange dont
le principal constituant est l’acétate de linalyle (ester peu soluble dans
l’eau).
►
Rôle du réfrigérant dans le montage du
chauffage à reflux :
-
Le réfrigérant permet de condenser les
vapeurs qui retournent à l'état liquide dans le ballon.
-
Il permet ainsi d’éviter les pertes de
matière par évaporation.
►
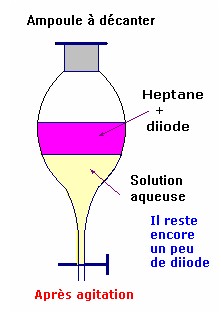
Extraction liquide / liquide :
-
Lors d’une extraction liquide/liquide :
-
L’espèce chimique à extraire est plus soluble
dans le solvant extracteur que dans le solvant de départ.
-
Et le solvant extracteur et le solvant de
départ sont non miscibles.
-
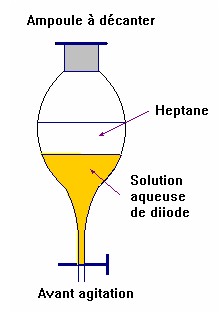
L’extraction par un solvant se réalise dans
une ampoule à décanter.
-
Le choix du solvant dépend de l’espèce
chimique recherchée.
-
Exemple :
extraction du diiode présent
dans une solution par l’heptane.
►
Extraction d’un produit liquide d’un mélange
réactionnel :
-
On peut réaliser une extraction liquide /
liquide à l’aide d’un solvant approprié.
-
On peut réaliser une distillation si les
constituants du mélange ont des températures d’ébullition différentes.
►
Chromatographie sur couche mince :
-
La
chromatographie est aussi une technique d’analyse.
-
Elle permet
d’identifier les espèces chimiques présentes dans un mélange.
-
Des espèces
chimiques identiques migrent à des hauteurs identiques sur une même plaque
de chromatographie.
►
Identification des solides :
-
On peut les identifier
ces solides en mesurant leur température de fusion (banc Kofler).

-
On peut réaliser une chromatographie sur
couche mince avec un éluant adapté.
-
La chromatographie
permet de séparer les espèces chimiques présentes dans un mélange homogène.
-
Elle est basée sur
la différence de solubilité d’une substance dans deux phases non miscibles :
-
Pour effectuer une
C.C.M, on utilise :
-
Une phase fixe sur
laquelle une goutte de mélange à séparer est déposée.
- La phase fixe est
constituée d’une mince couche de gel de silice déposée sur une plaque
d’aluminium.
-
Une phase
mobile ou éluant.
-
C’est le solvant
dans lequel les constituants du mélange sont plus ou moins solubles.
-
L’éluant migre le
long de la phase fixe grâce au phénomène de capillarité.
-
Il entraîne les
constituants du mélange qui se déplacent à des vitesses différentes.
-
On peut ainsi les
séparer.
-
La chromatographie
est aussi une technique d’analyse.
-
Elle permet
d’identifier les espèces chimiques présentes dans un mélange.
-
Des espèces
chimiques identiques migrent à des hauteurs identiques sur une même plaque
de chromatographie.
►
Rôle de l’éluant :
-
Il permet d’extraire ou de séparer les
espèces chimiques contenues dans le dépôt le long de la phase fixe.
►
Rendement de la synthèse :
-
Le rendement d’une synthèse, noté
ρ,
est égal au quotient
-
De la quantité de produit obtenu
nexp,
-
Par la quantité maximale de produit attendu
nmax.
-
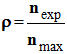
- La quantité maximale de de produit attendu
nmax est liée au réactif limitant.
►
Rendement de la synthèse :
-
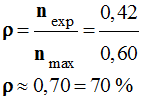
►
Quantité de produit obtenu
expérimentalement :
-
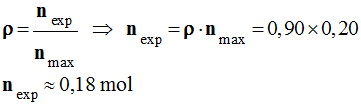
► Les nano-objets :
-
La taille : 10–10 m <
taille < 10–7
m
-
Leur taille leur confère des propriétés
particulières.
|
|