|
QCM N° 18 Pour s'auto-évaluer |
Composés organiques oxygénés |
|
|
|
|
QCM N° 18 : Composés organiques oxygénés
Pour chaque question,
indiquer la (ou les) bonne(s) réponse(s). |
|||||
|
|
Énoncé |
A |
B |
C |
R |
|
1 |
La classe d’un alcool dépend uniquement |
De la position du groupe hydroxyle |
De son nombre d’atome de carbone |
Du nombre d’atomes de carbone liés à l’atome de carbone fonctionnel |
C |
|
2 |
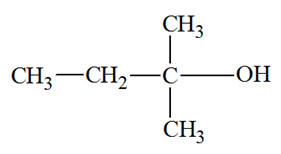
Cette molécule est un alcool : |
Primaire |
Secondaire |
Tertiaire |
A |
|
3 |
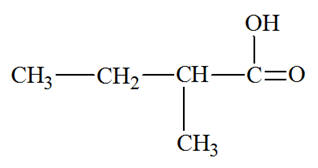
Cette molécule est un alcool : |
Primaire |
Secondaire |
Tertiaire |
C |
|
4 |
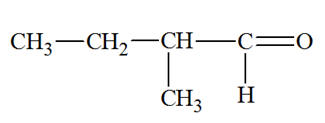
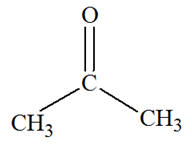
La molécule suivante :
|
Est un aldéhyde |
Est une cétone |
Est un composé carbonylé |
AC |
|
5 |
Une cétone comporte : |
Un atome de carbone fonctionnel relié à un atome d’hydrogène |
Un groupe carbonyle |
Un atome de carbone fonctionnel relié à deux atomes de carbone |
BC |
|
6 |
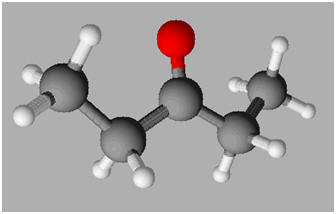
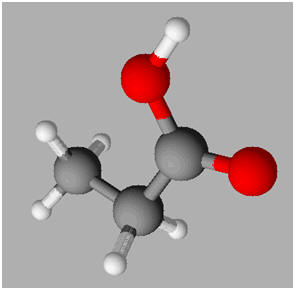
Ce modèle moléculaire est celui d’une molécule :
|
De pentanal |
De pentan-3-one |
De pentan-3-ol |
B |
|
7 |
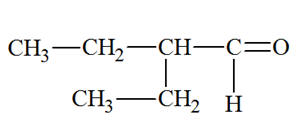
Le 2-éthylbutanal a pour formule semi-développée : |
|
|
|
A |
|
8 |
Ce modèle moléculaire est celui d’une molécule :
|
De propanal |
D’acide éthanoïque |
D’acide propanoïque |
C |
|
9 |
L’acide 2-méthylbutanoïque a pour formule semi-développée : |
|
|
|
B |
|
10 |
L’acide butanoïque C3H7–CO2H est plus soluble dans l’eau que : |
L’acide éthanoïque CH3–CO2H |
L’acide 2-méthylbutanoïque |
L’acide hexanoïque |
BC |
|
11 |
Le groupe carboxyle est un groupe : |
Hydrophile |
Hydrophobe |
Caractéristique des acides carboxyliques |
AC |
|
12 |
Le caractère acide de l’acide pentanoïque ou valérique est dû :
|
À la libération d’ions hydrogène par les molécules d’acide |
Au groupe carboxyle |
À l’ionisation des molécules d’acide |
ABC |
|
13 |
La molécule de formule semi-développée suivante est : CH3–CH2–CO2H |
Un alcool |
Un aldéhyde |
Un acide carboxylique |
C |
|
14 |
La molécule suivante possède le groupe caractéristique :
|
Hydroxyle |
Carbonyle |
Carboxyle |
B |
|
15 |
On oxyde la molécule A, ce qui permet d’obtenir une cétone. La molécule A est un alcool : |
Primaire |
Secondaire |
Tertiaire |
B |
|
16 |
On oxyde le benzaldéhyde C6H5–CHO par le dioxygène. On obtient la molécule de formule : |
C6H5–CH2 –OH |
C6H5–COOH |
C6H5–CH2–COOH |
B |
|
17 |
On oxyde 4,0 mol de benzaldéhyde en acide benzoïque. À la fin de la synthèse, on recueille 3,0 mol d’acide benzoïque. Le rendement ρ de la réaction est : |
ρ = 0,75 |
ρ = 1,3 |
ρ = 3,0
mol |
A |
- Définition des alcools :
- On appelle alcool tout composé organique possédant un groupe hydroxyle – OH lié à un atome de carbone tétragonal.
- Formule générale d’un alcool : R – OH.
- R est un groupement alkyl du type – CnH2n+1
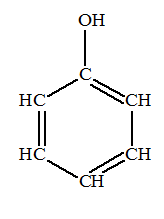
- Remarque : le phénol n’est pas un alcool, pourtant, il possède un groupe hydroxyle.
- Le carbone fonctionnel n'est pas tétragonal.
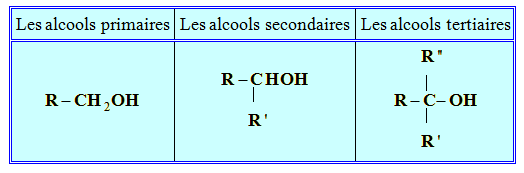
- Classe des alcools :
- On distingue :
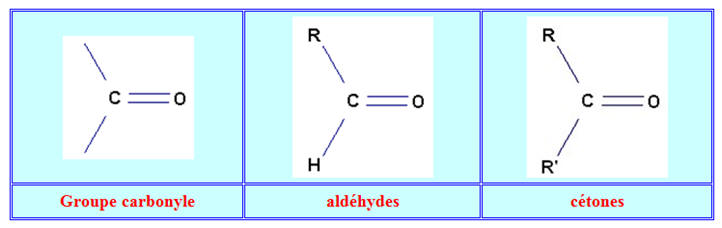
- Aldéhyde et cétone :
- Les aldéhydes et les cétones sont des composés carbonylés. Ils possèdent le groupe caractéristique :
- Le carbone fonctionnel est trigonal.
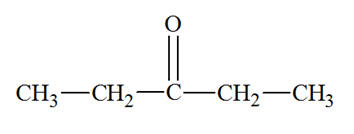
- La pentan-3-one
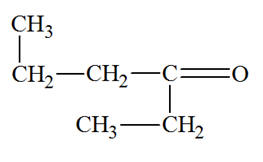
- Hexan-3-one :
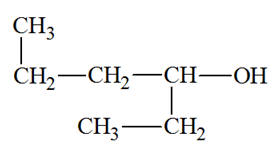
- Hexan-3-ol :
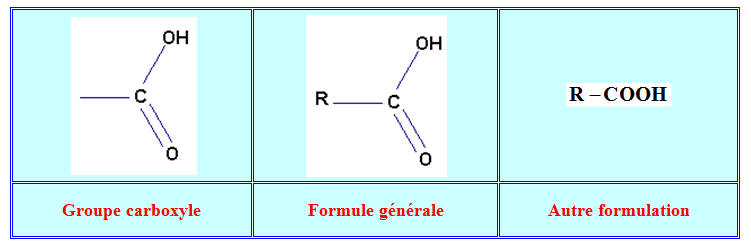
- Définition des acides carboxyliques.
-
Les acides carboxyliques
possèdent en commun le groupe caractéristique :
– COOH
- Le carbone fonctionnel est trigonal et il est lié à deux atomes d'oxygène.
- Formule semi-développée de la molécule d’acide propanoïque :
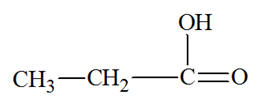
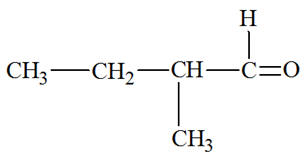
- Formule semi-développée du 2-méthylbutanal :
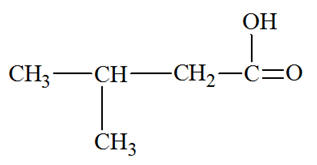
- Formule semi-développée de l’acide 3-méthylbutanoïque :
- Solubilité des acides carboxyliques :
- La solubilité dans l’eau d’un acide carboxylique est due au groupe carboxyle de cet acide, groupe hydrophile qui peut établir des liaisons hydrogène avec les molécules d’eau.
- La solubilité des acides carboxyliques R – CO2H dans l’eau diminue lorsque la taille du groupe hydrocarboné R, groupe hydrophobe, augmente.
- La solubilité d’un acide carboxylique augmente lorsque le pH croît.
- Les acides carboxyliques :
R
– COOH + H2O
= R –
COO–
+ H3O+
-
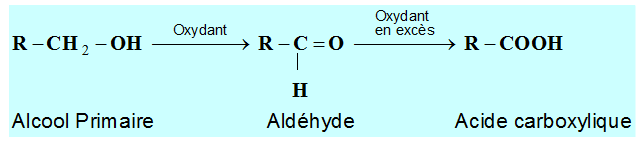
Oxydation des alcools
:
- L’oxydation d’un alcool primaire donne un aldéhyde en présence d’un excès d’alcool, ou un acide carboxylique en présence d’un excès d’oxydant.
- L’oxydation d’un alcool secondaire donne une cétone.
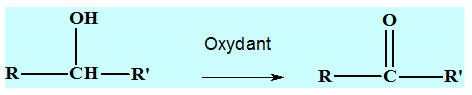
- Les alcools tertiaire ne sont pas oxydés (oxydation ménagée)
-
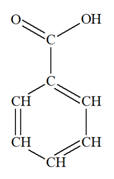
L’oxydation ménagée du
benzaldéhyde
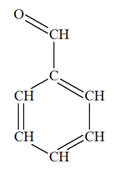 donne l’acide
benzoïque :
donne l’acide
benzoïque :
|
|