QCM N° 15 Le Gaz Parfait
|
|
 |
|
QCM N° 15
Modèle du gaz
parfait
AIDE
Pour chaque
question, indiquer la (ou les) bonne(s) réponse(s).
|
|
|
Énoncé
|
A
|
B
|
C
|
R
|
|
1
|
À température
T et
quantité de
matière n constantes,
la loi de
Mariotte s’écrit :
|
P
. T = cste
|
P
. V = cste
|
V
. T = cste
|
B
|
|
2
|
La pression d’un
gaz augmente
si la fréquence
des collisions
des entités du
gaz sur les parois
du récipient qui
le contient :
|
Diminue
|
Reste constante
|
Augmente
|
C
|
|
3
|
À température
constante,
si le volume d’un
échantillon
de gaz parfait
double,
sa pression :
|
Double
|
Est divisée
par 2
|
Ne varie pas
|
B
|
|
4
|
L’équation d’état
du
gaz parfait peut
se mettre
sous la forme :
|
P
. V . n = R . T
|
P
. V = n . R . T
|
P
. T = n . R . V
|
B
|
|
5
|
Le modèle du gaz
parfait
permet de décrire
le comportement
des gaz :
|
À basse
pression
|
À pression
élevée
|
Quelle que
soit la pression
|
A
|
|
6
|
D’après
l’équation d’état
du gaz parfait :
|
Si la pression
P
diminue,
la température
T
augmente
|
Si le volume
V
augmente,
la température
T
augmente,
à quantité de
n
matière
et pression
P
constantes
|
La pression P
est inversement
proportionnelle
à la quantité
de matière n
|
B
|
|
7
|
L’énergie interne
U
d’une phase
condensée
dépend :
|
De la pression
|
De la
température
|
De la nature
de la phase
condensée
|
BC
|
|
8
|
Les transferts
thermiques
se font
spontanément :
|
Depuis le
corps chaud
vers le corps
froid
|
Depuis le
corps froid
vers le corps
chaud
|
De manière
aléatoire
|
A
|
|
9
|
Le flux thermique
à
travers un mur
est
d’autant plus
grand que :
|
La différence
de température
entre l’intérieur
et l’extérieur
est grande
|
La différence
de température
entre l’intérieur
et l’extérieur
est petite
|
Le mur est
mal isolé
|
AC
|
|
10
|
La résistance
thermique
d’un mur en
béton :
|
Ne change pas
lorsqu’on
le couvre
de laine
de roche
|
Diminue une
fois couvert
de laine
de roche
|
Augmente une
fois couvert
de laine
de roche
|
C
|
QCM réalisé avec le logiciel Questy
Pour s’auto-évaluer

AIDE
Loi de Mariotte :
-
À température constante et pour une quantité donnée de gaz, le produit de la
pression P par le volume V occupé par le gaz est constant :
-
P
. V =
k = constante.
-
La loi de Mariotte est un modèle qui décrit correctement le comportement des gaz
aux faibles pressions.
-
Pour les grandes pressions, il existe d’autres modèles.
Force pressante et pression d’un gaz :
-
Les grandeurs macroscopiques de description du gaz (température T,
pression P, masse volumique ρ) reflètent le comportement
microscopique des entités chimiques (atomes, molécules ou ions) qui le
constituent.
-
La force pressante
résulte des chocs entre les entités, qui constituent le fluide, et les parois du
récipient.
-
Un fluide exerce une
force pressante sur les parois du récipient qui le contient .
-
La valeur de la force pressante
F dépend de la pression
P du fluide et de la surface de contact S :
|
F
= P . S
|
P :
Pression en N . m–2 ou pascal (Pa)
|
|
S :
Surface de contact en m2
|
|
F :
Force pressante en newton (N)
|
►
Équation d’état du gaz parfait :
-
Cette équation relie les différentes grandeurs macroscopiques qui permettent de
le décrire.
|
P . V
= n . R . T
|
|
P
|
Pression en
pascal (Pa)
|
|
V
|
Volume en mètre
cube (m3)
|
|
n
|
Quantité de
matière en mole (mol)
|
|
R
|
Constante du gaz
parfait :
R
= 8,314 Pa . m3 .mol–1 . K–1.
|
|
T
|
Température
absolue en kelvin (K)
|
-
Si la pression et la masse volumique du gaz sont trop importantes, alors le
modèle du gaz parfait n’est plus adapté.
Limites du modèle du gaz parfait :
-
Le modèle du gaz parfait est adapté :
-
Si la pression est faible ;
-
Si l’entité chimique, qui constitue le gaz, est
de faibles dimensions.
L’énergie interne U :
-
L’énergie interne est la somme des énergies cinétique et potentielle
microscopiques, c’est l'énergie liée à sa structure interne microscopique, notée
U.
-
Énergie interne : U (J)
-
Le plus souvent, on s’intéresse à la variation de l’énergie interne ΔU
d’un système.
-
L’énergie cinétique microscopique est lié à la vitesse de déplacement des
particules du système dans le référentiel d’étude.
-
Cette agitation augmente avec la température T, on l'appelle
l'agitation thermique.
-
Plus la température d’un système est élevée, plus l’agitation thermique des
particules qui le constituent est grande et plus son énergie cinétique
microscopique est grande.
-
L’énergie potentielle microscopique est due aux interactions gravitationnelle,
électromagnétique, forte et faible entre les particules qui constituent le
système.
-
On distingue les énergies potentielles microscopiques chimique, électrique,
magnétique et nucléaire.
-
Les énergies potentielles résultent de l’énergie de liaisons chimiques et de
l’énergie de masse des noyaux.
-
On peut citer d’autres formes d’énergies potentielles microscopiques qui
résultent de liaisons intermoléculaires entre les molécules qui constituent le
système étudié.
-
Ces énergies potentielles microscopiques varient lors d’un changement d’état de
la matière : fusion, liquéfaction, solidification.
Le transfert thermique Q :
-
Le transfert thermique est de l'énergie cinétique d'agitation des
particules qui composent le système ; mais cette agitation est désordonnée.
-
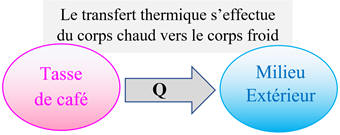
Ainsi, lorsqu’il existe une différence de température entre le système et le
milieu extérieur, le transfert thermique Q se fait spontanément du corps
le plus chaud vers le corps le plus froid.
-
Le transfert thermique est une forme d'énergie.
-
Cas d’une tasse de café
(65 ° C) qu’on laisse à la température ambiante (21 ° C).
-
Au cours du temps, la température du café diminue.

-
La tasse de café constitue le système d’étude S, l’autre système S’
est constitué par le milieu extérieur.
-
Un transfert d’énergie s’effectue de la tasse de café vers le milieu extérieur.
-
La tasse de café cède de l’énergie sous forme de transfert thermique, notée Q,
au milieu extérieur.
Le flux thermique :
-
Le flux thermique Φ (phi majuscule) caractérise la vitesse du transfert
thermique Q pendant une durée Δt au
sein d’un système ou entre différents systèmes.
-
On considère un matériau dont les deux faces parallèles numérotées 1 et 2, de
même surface S, sont à des températures différentes T1
et T2, telles que T1 > T2.
-
La paroi plane, dont deux faces sont à des températures différentes T1
et T2, est le siège d’un transfert thermique par conduction.
-
La capacité d’un matériau, à réaliser plus ou moins rapidement ce transfert, est
liée à sa résistance thermique Rth.
-
L’énergie Q est transférée de la face 1 vers la face 2 pendant la durée
Δt.
-
Le flux thermique Φ traversant ce matériau est alors défini par la
relation :
|
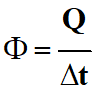
|
|
Énergie thermique transférée :
Q en joule (J)
|
|
Durée : Δt
ne seconde (s)
|
|
Flux thermique : Φ en watt : (J . s–1 = W)
|
-
Le flux thermique a la dimension d’une
puissance : c’est une énergie par unité de temps.
-
Le flux thermique est l’énergie transférée à travers une paroi par unité de
temps.
-
Ce transfert se fait spontanément de la source chaude vers la source froide.
-
Ce transfert est naturellement irréversible.
-
Par convention, le flux thermique est compté :
-
Positivement
s’il est reçu par le système S ;
-
Négativement
s’il est cédé par le système S.
-
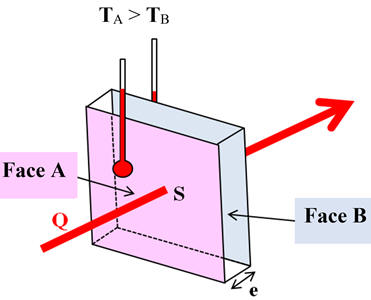
Cas d’une résistance thermique Rth :
-
La résistance thermique Rth caractérise l’opposition d’un milieu au transfert
thermique entre deux points A et
B.
-
On considère le système S de résistance thermique Rth
:
-
On oriente le flux thermique du point A
vers le point B.
-
Si l’écart de température TA – TB est
maintenu constant, le flux thermique est donné par la relation suivante :
|
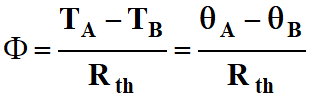
|
|
Températures absolues : TA
et TB en
kelvin (K)
Ou températures θA
et θB en degré Celsius (° C)
|
|
Résistance
thermique : Rth
unité : (K . W–1) ou (° C . W–1).
|
|
Flux
thermique : Φ en watt : (J . s–1
= W)
|
Résistance thermique (suite) :
-
Remarque :
-
Plus la résistance thermique du matériau est élevée, plus le flux thermique est
faible à travers le matériau.
-
Ce dernier empêche le transfert d’énergie à travers lui ; c’est de ce fait un
bon isolant thermique.
-
Un matériau qui a une résistance thermique élevée est un bon isolant thermique.
-
La laine de roche est un bon isolant thermique.