|
TP Chimie. N° 02 |
Extraction. Correction. |
|
|
Programme 2010 : Programme 2020 : |
|
|
|
But :
expérimenter
quelques techniques d’extraction. |
|
Matériel :
élèves :
|
6 tubes à essais - 6 bouchons – solution de sulfate de cuivre – huile – heptane – dichlorométhane (ou chlorure de méthylène) |
|
Prof : |
1 ampoule à décanter – 1 éprouvette graduée – 2 béchers – du papier sulfurisé – essence de lavande – eau distillée – solution de chlorure de sodium à 40 g / L – un montage pour l’hydrodistillation. |
a)- Mode opératoire :
b)- Observations :
Cliquer sur l'image pour l'agrandir
c)- Conclusion : La nature du liquide qui surnage dépend-elle des volumes utilisés ?
De la nature des deux liquides ?
|
- La nature du liquide qui surnage ne dépend pas des volumes de solutions utilisées. - La disposition des deux liquides dépend de la nature des deux liquides. - Lorsque l'on agite, il se produit une émulsion. - Après décantation, on retrouve les deux liquides dans les mêmes positions. - L'huile et la solution aqueuse de sulfate de cuivre II sont des liquides non miscibles. - L'huile est moins dense que la solution aqueuse de sulfate de cuivre II. - Il en est de même pour l'heptane et la solution aqueuse de sulfate de cuivre II. - La solution de dichlorométhane est plus dense que la solution aqueuse de sulfate de cuivre II. - De plus les deux solutions sont non miscibles. |
![]() Verser 2 mL de solution de diiode dans un tube à
essais, ajouter délicatement 2 mL d’heptane. Observer, puis agiter.
Verser 2 mL de solution de diiode dans un tube à
essais, ajouter délicatement 2 mL d’heptane. Observer, puis agiter.
![]() Décrire le phénomène observé et conclure.
Décrire le phénomène observé et conclure.
Cliquer sur l'image pour l'agrandir
|
- Avant agitation : - On verse la solution d'heptane (solution incolore) délicatement. - On remarque que la solution aqueuse de diiode (jaune orangée) et la solution d'heptane (incolore) sont non miscibles. - L'heptane est moins dense que la solution aqueuse de diiode (lugol), il se situe au-dessus. - Après agitation, l'heptane prend une coloration violette et la solution aqueuse de diiode prend une teinte jaune clair. - Interprétation : - Le diiode est plus soluble dans l'heptane que dans l'eau. - Lors de l'agitation, il passe de la phase aqueuse (solution aqueuse de diiode) à la phase organique (solution d'heptane). - On a réalisé une extraction par un solvant (ici l'heptane). |
- Cette technique, basée sur la non-miscibilité de certains liquides, utilise le fait qu’en phase gazeuse, toutes les espèces sont miscibles.
- Les molécules organiques composant l’essence de lavande sont entraînées avec la vapeur d’eau.
- L’ensemble est condensé puis récupéré
dans une éprouvette graduée.
![]() Introduire 30 g de fleur de lavande dans un ballon à fond rond (250 mL).
Ajouter 100 mL d’eau distillée environ.
Introduire 30 g de fleur de lavande dans un ballon à fond rond (250 mL).
Ajouter 100 mL d’eau distillée environ.
- Réaliser le montage, adapter le réfrigérant et porter le mélange à l’ébullition.
- Maintenir
le chauffage jusqu’à obtention de 60 mL de distillat.
|
(1)‑
Chauffe-ballon. (2)‑ Mélange. (3)‑ Thermomètre. (4)‑ Réfrigérant oblique. (5)‑Arrivée et Sortie de l’eau. (6)‑ Éprouvette. (7)‑ Fleur de lavande. (8)‑ Huile essentielle.
|

Vidéo (zoom)
![]() Faire un schéma légendé et détaillé
du montage.
Faire un schéma légendé et détaillé
du montage.
- décrire succinctement l’expérience.
-
Indiquer les différentes observations faites
au cours de l’expérience.







- Qu’observe-t-on dans l’éprouvette graduée ?
- Proposer une méthode de séparation des deux produits.
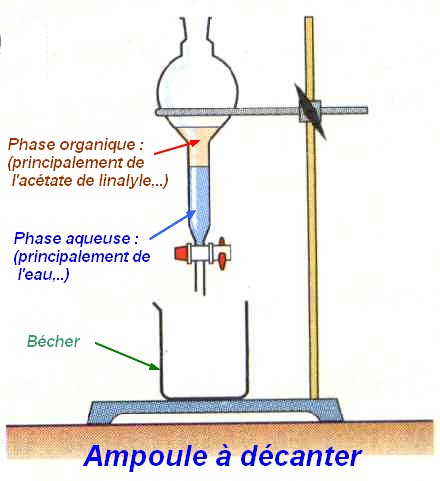
- On utilise une ampoule à décanter pour séparer les deux phases :
- La phase aqueuse et la phase organique (essence de lavande).
|
- Dans l’éprouvette graduée se trouvent de l’eau et de l’essence de lavande qui est principalement constituée d’acétate de linalyle. - On va utiliser le fait que l’acétate de linalyle (produit que
l’on veut extraire) est très peu soluble dans l’eau salée. |
![]() Mode opératoire :
Mode opératoire :
|
- Verser le contenu de l’éprouvette dans une ampoule à décanter. - Ajouter environ 10 mL d’eau salée. Agiter, laisser décanter. - Récupérer la phase supérieure en la dissolvant dans du dichlorométhane (solvant organique). - On conserve cette solution pour la prochaine séance de travaux pratiques. |
![]() Faire les schémas légendés des diverses manipulations réalisées
en indiquant le matériel utilisé.
Faire les schémas légendés des diverses manipulations réalisées
en indiquant le matériel utilisé.
Additif :
► Voici une partie de la fiche technique de l’essence de lavande produite par la
GAEC LES Grandes marges Valensole.
- Désignation : Lavande (Maillette)
- Chromatogramme : Proportion relative des principaux constituants (%).
|
limonène |
0,2 |
octanone-3 |
0,81 |
terpinène - 4 - ol |
4,57 |
|
eucalyptol |
0,62 |
camphre |
0,21 |
bornéol |
0,58 |
|
cis-béta-ocimène |
5,43 |
linalol |
27,69 |
acétate de lavandulyle |
3,97 |
|
trans-béta-ocimène |
3,09 |
acétate de linalyle |
34,84 |
lavandulol |
0,85 |
|
alpha - terpinéol |
0,42 |
|
|||
|
Principaux
constituants |
% |
On peut réaliser un histogramme
à l’aide d’un tableur (Excel). On peut facilement remarquer, grâce au graphique obtenu que le constituant le plus abondant est l’acétate de linalyle, puis le
linalol, etc.….. |
|
limonène |
0,2 |
|
|
eucalyptol |
0,62 |
|
|
cis-béta-ocimène |
5,43 |
|
|
trans-béta-ocimène |
3,09 |
|
|
octanone-3 |
0,81 |
|
|
camphre |
0,21 |
|
|
linalol |
27,69 |
|
|
acétate de linalyle |
34,84 |
|
|
terpinène - 4 - ol |
4,57 |
|
|
bornéol |
0,58 |
|
|
acétate de lavandulyle |
3,97 |
|
|
lavandulol |
0,85 |
|
|
alpha - terpinéol |
0,43 |
|
|
Autres |
16,71 |
|