|
|
|
Objectifs :
-
Mesurer
la conductance d’une portion de solution électrolytique.
- Étudier
quelques facteurs influençant la conductance |
|
TP Chimie N° 05 |
Conductance et facteurs d’influence. Correction. |
|
|
|
|
Objectifs :
-
Mesurer
la conductance d’une portion de solution électrolytique.
- Étudier
quelques facteurs influençant la conductance |
|
Matériel : Un G.B.F, deux multimètres (un noir et un jaune), 5 cellules de conductimétrie, des fils de connexion, des béchers, Des solutions : (Na+ + Cl – ) (C1 = 2,0 x 10 – 3 mol / L ; C = 5,0 x 10 – 3 mol / L ; C2 = 1,0 x 10 – 2 mol / L), (Na+ + HO – ) et (H+ + Cl – ), (C = 5,0 x 10 – 3 mol / L ). |
|
II- Facteurs influençant la conductance. |
- Dans une solution aqueuse électrolytique, le passage du courant électrique est assuré par le déplacement des ions.
- On s’intéresse au caractère conducteur d’une solution électrolytique.
- Dans certaines conditions, une solution ionique se comporte comme un conducteur ohmique.
- Elle répond alors à
-

- R est une grandeur caractéristique du conducteur.
- Elle rend compte de la capacité de celui-ci à s’opposer au passage du courant (d’où son nom).
- Les chimistes préfèrent étudier l’inverse c’est-à-dire la capacité qu’a la solution électrolytique à laisser passer le courant.
- Ils étudient la conductance G qui est l’inverse de la résistance :
- 
- Loi d’Ohm :
- 
a)- Principe.
- Pour déterminer la valeur de G, on utilise la loi d’Ohm :
-

- Il faut connaître U et I.
- Pour cela, on plonge dans la solution ionique, deux plaques métalliques, appelées électrodes, reliées à un générateur.
- On mesure la tension U entre les électrodes avec un voltmètre.
- On mesure l’intensité I du courant dans le circuit avec un ampèremètre.
- L‘ensemble constitué par les deux plaques métalliques planes et parallèles est appelé : Cellule conductimétrique.
- On détermine ensuite la valeur de la conductance G de la portion de solution ionique comprise entre les électrodes.
b)- Dispositif expérimental : Prendre l’électrode S
=
- Schéma :
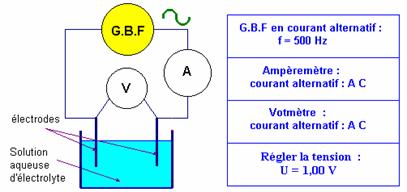
![]() Réaliser le montage et les différents réglages avant de
rincer les électrodes.
Réaliser le montage et les différents réglages avant de
rincer les électrodes.
c)- Mesure :
![]() Rincer les électrodes à l’eau distillée. Éliminer l’eau
de rinçage délicatement avec du papier absorbant.
Rincer les électrodes à l’eau distillée. Éliminer l’eau
de rinçage délicatement avec du papier absorbant.
- Agiter doucement la cellule dans la solution pour bien homogénéiser.
- La solution ionique est une solution de chlorure de sodium de concentration C = 5,0 x 10 – 3 mol / L.
- Réaliser une mesure de G.
-
Avant chaque mesure, il faut rincer
les électrodes à l’eau distillée. - Essuyer délicatement les électrodes avec du papier absorbant, -
Agiter doucement la cellule dans la solution
pour bien homogénéiser. |
Animation CabriJava
Cliquer sur l'image pour l'agrandir
II- Facteurs influençant la conductance.
1)- Influence des caractéristiques S et ℓ de la cellule.
- On dispose d’un jeu de cellules conductimétriques.
- On peut faire varier la distance ℓ entre les électrodes et la surface S de leur partie immergée.
a)- Influence de la distance ℓ entre les électrodes.
- Faire une mesure avec
S =
- Comparer la valeur de cette mesure à celle obtenue au I- 2)- c)-. Conclusion.
|
-
On prend des électrodes de
surfaces
S
= 1 cm2 que l’on éloigne.
- Conclusion :
-
La
conductance
G diminue, lorsque la distance
ℓ
entre
les électrodes augmente. |
b)- Influence de S.
-
la distance
ℓ entre les électrodes
étant maintenue constante (ℓ
=
- Faire une mesure et la comparer à la valeur obtenue au
I- 2)- c)-. (S = 1 cm2 et
ℓ =
|
-
On prend des électrodes que
l’on garde à la même distance
ℓ
=
- Conclusion :
-
La
conductance
G augmente, lorsque la surface
S
augmente. |
2)- Influence des caractéristiques de la solution.
- On utilise la cellule conductimétrique du I- 2)- b)-dont les dimensions sont fixées.
- On peut ainsi mettre en évidence des grandeurs d’influence propres à la solution.
a)- Influence du soluté.
- On dispose de solutions (Na + + Cl – ) ; (Na + + HO– ) ; (H + + Cl – ) de même concentration : C = 5,0 x 10 – 3 mol / L.
![]() Réaliser les mesures puis reproduire et compléter le tableau
suivant.
Réaliser les mesures puis reproduire et compléter le tableau
suivant.
|
Solution |
(Na+ + Cl – ) |
(Na+ + HO – ) |
(H+ + Cl – ) |
|
G en mS |
|
|
|
![]() Conclusion.
Conclusion.
|
- On dispose de solutions aqueuses de chlorure de sodium, - de soude - et d’acide chlorhydrique - de même concentration : - C = 5,0 x 10 – 3 mol / L.
On mesure la conductivité de chaque solution avec la même
cellule conductimétrique.
- Conclusion :
- La
conductance
G d’une portion de solution, dépend de la nature du soluté, c’est-à-dire
des ions présents dans la solution. |
b)- Influence de la concentration.
- On dispose de la solution (Na+ + Cl – ) de concentration :
- C1 = 2,0 x 10 – 3 mol / L ; C = 5,0 x 10 – 3 mol / L ; C2 = 1,0 x 10 – 2 mol / L.
![]() Réaliser les différentes mesures, reproduire et compléter le
tableau.
Réaliser les différentes mesures, reproduire et compléter le
tableau.
|
C mmol / L |
2 |
5 |
10 |
|
G mS |
|
|
|
![]() Conclusion.
Conclusion.
|
-
On dispose de solutions
aqueuses de chlorure de sodium de différentes concentrations.
-
La conductance
G
augmente quand la concentration molaire en soluté apporté augmente. |
c)- Influence de la température.
- Relever la température θ de la solution (Na+ + Cl – ) de concentration C = 5,0 x 10 – 3 mol / L :
- θ =
- faire chauffer la solution et relever la température q’ de cette solution.
- θ ’ =
- réaliser la mesure et comparer la valeur obtenue à celle du I- 2)- c)-. Conclusion.
|
- On mesure la conductance d’une solution de chlorure de sodium de concentration C = 5,0 x 10 – 3 mol / L à différentes températures.
On utilise toujours la même cellule conductimétrique.
- Conclusion : La conductance augmente avec la température θ. |
|
► Récapitulatif : |
|
|
► La conductance G dépend |
|
|
- De la distance ℓ entre les électrodes, |
- Lorsque la distance ℓ augmente, la conductance G diminue |
|
- De la surface S des électrodes, |
- Lorsque la surface S augmente, la conductance G augmente |
|
- De la nature des ions présents dans la solution, |
- Pour un même cation (Na+), la conductance d’une solution contenant les ions hydroxyde est supérieure à celle d’une solution contenant des ions chlorure de même concentration. - Pour un même anion (Cl – ), la conductance d’une solution contenant les ions oxonium est supérieure à celle d’une solution contenant des ions sodium de même concentration. |
|
- De la concentration C de la solution, |
- Lorsque la concentration C augmente, la conductance G augmente |
|
- De la température θ de la solution. |
- Lorsque la température θ augmente, la conductance G augmente |