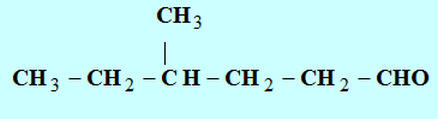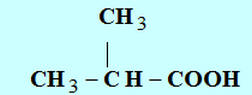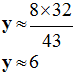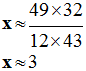|
Contrôle N° 05 Avril 2000 Première S énoncé et correction |
|
|
|
|
1)- Écrire les formules semi-développées des composés suivants : a)- 2,2-diméthylbutanol b)- 4-méthylhexanal c)- 3,3-diméthylbutanone d)- acide méthylpropanoïque |
|
Correction |
|
|
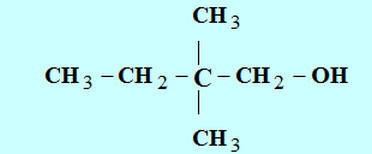
a)-
2,2-diméthylbutanol |
|
|
b)-
4-méthylhexanal |
|
|
c)-
3,3-diméthylbutanone |
|
|
d)- acide
méthylpropanoïque |
|
|
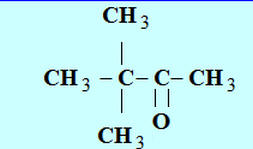
2)- Nommer les composés suivants : a)-
b)-
c)-
|
|
Correction |
||
|
a)-
2,2-diméthylbutanal |
b)-
acide 2,2-diméthylbutanoïque |
c)-
3-méthylbutan-2-one |
|
1)- équilibrer l'équation bilan suivante :
Ag(NH3)2+
+ HO – +
CH3CHO
→ Ag +
CH3COO –
+ H2O +
NH3 - Dans un premier temps, il faut écrire les demi-équations électroniques en indiquant l'oxydant et le réducteur. - Puis d'en déduire l'équation bilan en indiquant clairement la méthode utilisée. |
|
|
|
2 ( |
e– |
+ |
Ag(NH3)2+ |
= |
|
|
Ag |
|
+ |
2 NH3 |
) |
|
1 ( |
CH3CHO |
+ |
3
HO
– |
|
|
= |
CH3COO
– |
|
|
+ 2
H2O |
+ |
2 e– |
) |
|
---------------------------------------------------------------------------------------------------------- |
|||||||||||||
|
|
CH3CHO |
+ |
3
HO
– |
+ |
2
Ag(NH3)2+ |
→ |
CH3COO
– |
+ |
2 Ag |
+ 2
H2O |
+ |
4
NH3 |
|
|
2)- L'analyse d'un composé organique donne le pourcentage en masse des éléments suivants : carbone, 49 % ; hydrogène, 8,0 % ; oxygène : 43 %. a)- Montrer que le composé chimique ne contient que les éléments carbone, oxygène et hydrogène. b)- Déterminer la formule brute de ce composé sachant qu'il possède un groupement carboxyle et un radical alkyle. c)- Écrire la formule semi-développée et donner le nom.
M (C) = 12
g / mol ; M
(H) = 1,0 g / mol ;
M
(O) = 16 g /
mol |
|
Correction : |
||||||||||||
|
a)- Le
composé ne contient que les éléments carbone, oxygène et
hydrogène car :
% C
+ % O
+ % H = 49 + 43 + 8 = 100 b)- La formule de la molécule est du type : R – COOH, R étant un radical alkyle du type – CnH2n+1.
On peut écrire la formule de la molécule sous la forme
suivante : CxHyO2
Valeur de
y :
Valeur de x :
Formule brute : C3H6O2 ;
C2H5COOH
c)- Formule
développée et nom On en déduit la
formule :
CH3
– CH2
– COOH
acide propanoïque |