|
TP Chimie N° 08 :
Stéréochimie :
Conformation et configuration |
|
|
|
Matériel : modèles moléculaires et miroir.
I- Notions de base.
1)- Donner les différentes structures de l'atome de carbone.
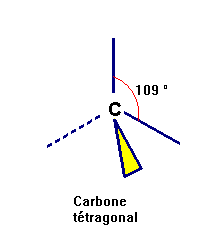
Le carbone tétragonal : il échange 4 liaisons simples avec 4 atomes ou groupe d'atomes distincts.
Il possède 4 voisins.
On parle de carbone tétraédrique car l'atome de carbone est situé au centre d'un tétraèdre.
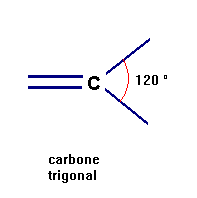
Le carbone trigonal : il échange 2 liaisons simples et une double liaison.
Il possède 3 voisins.
Il se trouve au centre d'un triangle dont les trois voisins occupent les sommets.
2)- Donner la représentation conventionnelle.
Représentation de CRAM du carbone tétragonal.
- un trait plein représente une liaison entre deux atomes situés dans le plan de la figure.
- un triangle allongé représente une liaison entre un atome situé dans le plan de la figure et un atome situé en avant de ce plan.
- un trait pointillé représente une liaison entre un atome situé dans le plan de la figure et un atome situé en arrière de ce plan.
Représentation conventionnelle du carbone trigonal :
II- Isomérie et isomères.
Deux molécules isomères sont deux composés qui ont la même formule brute mais dont les molécules sont différentes.
Les molécules de deux isomères ne sont pas superposables.
III- Isomérie de constitution et stéréoisomères.
1)- Isomérie de constitution.
- Deux isomères de constitution différent par la nature ou l'ordre des liaisons qui relient les atomes entre eux.
Ils n'ont pas la même formule développée ou semi-développée plane.
- On distingue :
l'isomérie de chaîne ( les molécules diffèrent par leur chaîne carbonée)
l'isomérie de position ( un groupe caractéristique ou une insaturation occupe une position différente sur un même squelette carbonée)
l'isomérie de fonction ( les molécules présentes des groupes fonctionnels différents ).
2)- Formule de constitution.
- Un isomère de constitution est parfaitement déterminé lorsque l'on connaît son squelette carboné.
- La formule plane, appelée formule de constitution indique la nature et l'enchaînement des liaisons entre les atomes de la molécule. On distingue :
- La formule développée plane.
- La formule semi-développée plane.
- La formule topologique.
Les isomères de constitution sont des corps purs différents qui possèdent des propriétés physiques et chimiques différentes.
3)- Application.
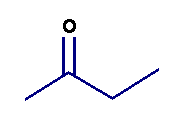
a)- Donner la formule développée plane, la formule semi-développée et la formule topologique de la molécule suivante : butan-2-one.
b)- Donner les formules semi-développées et les formules topologiques des différents isomères des molécules suivantes : C4H10 et C3H8O.
Préciser le type d'isomérie rencontré et le nom de chaque molécule.
Réponses :
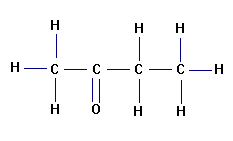
a)- La butanone :
Formule
développée
:
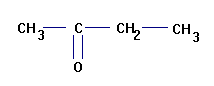
Formule
semi-développée
Formule
topologique
b)- Le butane :
|
Le butane |
|
|
|
L'isobutane |
2-méthylpropane |
|
|
isomérie de chaîne |
||
Les alcools : le propan-1-ol (alcool primaire) et le propan-2-ol (alcool secondaire).
|
Le propanol ou propan-1-ol |
alcool primaire |
|
|
le propan-2-ol |
alcool secondaire |
|
|
|
Isomérie de position entre les deux alcools. |
|
|
le méthoxyéthane |
éther |
|
|
Isomérie de fonction entre les alcools et l'éther |
||
IV- La stéréoisomères.
1)- Définition.
Deux corps sont stéréoisomères lorsqu'ils ont :
- Même constitution (même formule plane).
- Mais des structures spatiales différentes
Ils différent par l'agencement spatial de leurs atomes.
- On distingue :
- Les stéréoisomères de conformation.
- Les stéréoisomères de configuration.
2)- Conformations de l'éthane.
a)- Définition :
- On appelle conformation d'une molécule les différentes structures spatiales qu'elle peut prendre par suite de la rotation autour de ses liaisons simples.
b)- Projection de NEWMAN :
- Construire la molécule d'éthane.
- Noter a et b chaque atome de carbone.
- Regarder la molécule suivant l'axe de la liaison carbone-carbone.
- Représenter les deux conformations remarquables (conformation décalée et conformation éclipsée).
Réponses :
Formule semi-développée de
la molécule d'éthane :
![]()
|
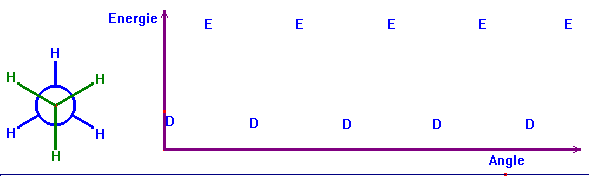
Conformation décalée D |
|
Conformation éclipsée E |
Le conformère E et le conformère D sont des stéréoisomères de conformation.
A température ambiante, il y a libre rotation autour de la simple liaison.
Le passage de l'un à l'autre se fait sans rupture de liaison.
c)- Aspect énergétique.
- Laquelle des deux conformations est la plus stable ?
3)- Isomérie de configuration. Isomérie Z et E.
a)- Cas du but-2-ène.
- Construire la molécule.
- Donner la formule semi-développée et la formule topologique des isomères Z et E.
- Comment passe-t-on d'un isomère à l'autre ?
|
|
|
|
(E) but-2-ène Entgegen (en face, opposé), les hydrogènes sont situés de part et d'autre de la double liaison |
(Z) but-2-ène Zusammen (ensemble), les hydrogènes sont situés du même côté de la double liaison. |
Le (Z) but-2-ène et le (E) but-2-ène sont des stéréoisomères de configuration.
Ce sont des corps purs distincts.
Il n'y a pas libre rotation autour de la double liaison à température ambiante.
Pour passer d'un stéréoisomère à l'autre, il faut rompre une liaison chimique.
b)- Conclusion.
- Le passage d'un stéréoisomère de conformation à l'autre se fait sans rupture de liaison.
- Le passage d'un stéréoisomère de configuration à un autre nécessite la rupture d'une liaison chimique.
- Les isomères Z et E sont des corps purs distincts que l'on peut isoler.
- Ils ont des propriétés physiques, chimiques, biologiques différentes.
V- L'énantiomérie. (Isomérie de configuration).
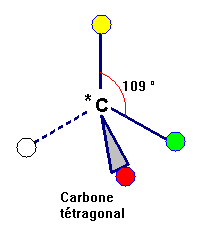
1)- Le carbone asymétrique.
C'est un atome de carbone tétragonal lié à quatre atomes ou groupes différents.
On le repère par un astérisque.
2)- Les énantiomères.
- Construire une molécule A possédant :
- Un carbone asymétrique et quatre groupes différents (prendre une boule rouge, une verte, une boule jaune et une boule blanche).
- Placer la liaison carbone-boule jaune verticalement.
- Donner la représentation conventionnelle de la molécule en mettant en évidence le carbone asymétrique.
- Mettre la molécule A devant un miroir et construire la molécule B image de A dans le miroir.
- Représenter les deux molécules A et B à l'aide de la représentation conventionnelle. Les molécules A et B sont-elles superposables ?
Réponse :
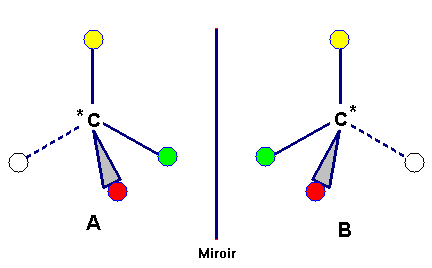
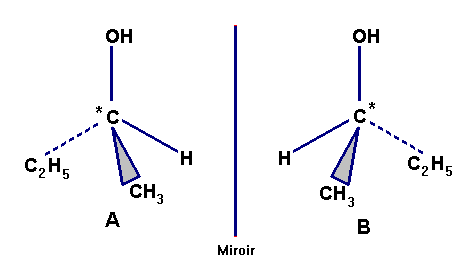
Les molécules A et B ne sont pas superposables, elles sont image l'une de l'autre dans un miroir.
Ce sont des stéréoisomères de configuration, on dit aussi des énantiomères.
- Définir l'énantiomérie.
L'énantiomérie est la relation existant entre deux isomères de configuration, image l'un de l'autre dans un miroir et non superposables.
Les isomères correspondants sont appelés énantiomères.
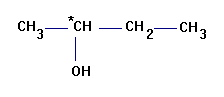
- Exercice : la molécule de butan-2-ol possède-t-elle un carbone asymétrique ? Si oui représenter les deux énantiomères.
3)- La chiralité.
- La chiralité est la propriété d'un objet de ne pas être superposable à son image dans un miroir.
- Donner un exemple d'un objet chiral. (une main)
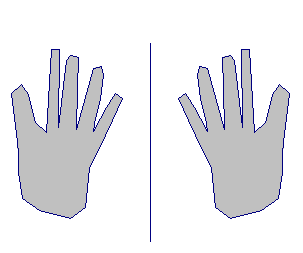
- Une molécule est chirale si elle possède un carbone asymétrique.
- On appelle mélange racémique un mélange de quantités égales de deux énantiomères.
4)- Énantiomérie et propriétés.
- Les énantiomères présentent très souvent des propriétés physiques et chimiques identiques.
- Par contre les propriétés biologiques et pharmacologiques de deux énantiomères sont presque toujours différentes.
- deux énantiomères n'ont pas le même effet sur la lumière polarisé rectilignement.
- La solution d'une substance chirale peut faire tourner le plan de polarisation de la lumière, on dit que cette substance est optiquement active.
- Elle possède un pouvoir rotatoire.
- Une substance qui fait tourner le plan de polarisation de la lumière dans le sens des aiguilles d'une montre est dite dextrogyre notée ( + ).
- Une substance qui fait tourner le plan de polarisation de la lumière dans le sens trigonométrique est dite lévogyre notée ( - ).
- L'angle de rotation du plan de polarisation est appelé pouvoir rotatoire.
- Deux énantiomères ont des pouvoirs rotatoires opposés. Un mélange racémiques ne possède pas de pouvoir rotatoire.
VI- Applications.
1)- À partir du tableau donner la définition des termes et expressions suivants :
Isomères de constitution, stéréoisomères, isomères de fonction, isomères de position,
isomères de configuration, isomères de conformation, diastéréoisomères, énantiomères.
Réponses :
|
Les molécules A et B ont la même formule brute, mais ne sont pas superposables
|
|||||||||
|
|
|
|
|||||||
|
A et B sont isomères de constitution |
NON
|
A et B ont-elles la même formule développée plane ? |
OUI
|
A et B sont stéréoisomères |
|||||
|
|
|
|
|
||||||
|
|
A et B présentent-elles la même fonction chimique ? |
|
A et B peuvent-ils être interconvertis par des rotations autour de liaisons simples ? |
|||||
|
|
|
|
|
|
|
|||
|
|
A et B sont isomères de fonction |
A et B sont isomères de position ou de chaîne |
|
A et B sont isomères de configuration |
A et B sont isomères de conformation |
|||
|
|
|
|
|
|
|
|
||
|
|
A et B présentent-ils le même squelette carbonée ? |
|
A et B sont-ils image l'un de l'autre dans un miroir? |
|||||
|
|
|
|
|
|
|
|||
|
|
A et B sont isomères de chaîne
|
A et B sont isomères de position |
A et B sont diastéréoisomères. Exemple : l'isomérie Z et E |
A et B sont énantiomères Exemple : présence d'un carbone asymétrique, molécule chirale. |
||||
|
|
|
|
|
|
|
|
|
|
- Isomères de constitution : molécules ayant la même formule brute.
Les molécules n'ont pas la même formule développée plane et ne sont pas superposables.
- Stéréoisomères : molécules ayant la même formule brute.
Les molécules ont la même formule développée plane mais ne sont pas superposables.
- Isomères de fonction : isomères de constitution n'ayant pas la même fonction chimique.
- Isomères de position : isomères de constitution qui différent par la position des substituants sur la chaîne carbonée.
- Isomères de configuration : stéréoisomères qui peuvent être interconvertis par rotation autour de simples liaisons.
- Isomères de configuration : stéréoisomères qui peuvent être interconvertis par la rupture puis la formation de liaisons chimiques.
- Diastéréoisomères : stéréoisomères de configuration qui ne sont pas image l'un de l'autre dans un miroir (isomérie Z et E).
- Énantiomères : stéréoisomères de configuration qui sont image l'un de l'autre dans un miroir.
2)- Exercices : 10, 12, 15 pages 220, 221.
- Exercice 10 page 220 :
|
|
|
|