|
Dipôle électrique et Moment dipolaire. Cours. |
|
|
|
Dipôle électrique (construction géométrique) |
|
|
|
-
ADDITIF : Dipôle
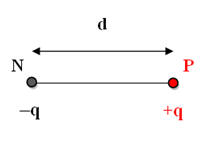
électrique et Moment dipolaire. - Un dipôle électrique est constitué de deux charges électriques opposées + q et –q, situées respectivement aux points P et N
de l’espace et distante de d. -
Représentation :
-
À ce dipôle est associé un moment dipolaire
-
Caractéristiques du moment dipolaire : -
Le moment dipolaire est représenté par un
segment fléché tel que : -
Le point d’application est le point N -
La direction : la droite (NP) -
Le sens de N vers P (du – vers
le +) -
La valeur : p = q . d = q . NP -
Expression vectorielle : -
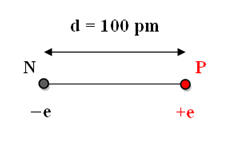
Exemple : on considère deux charges + e
et – e séparées par une distance de 100
pm -
(e = 1,60
× 10–
19 C) -
Calculer la valeur du moment dipolaire créé
par ce dipôle
-
Valeur du moment dipolaire : -
p = q . d ≈ 1,60
× 10 –
19
× 100
×
10 –
12 -
p ≈ 1,60
× 10 –
29 C.m
-
On utilise une autre unité pour exprimer la
valeur du moment dipolaire. -
On utilise de debye, de symbole D : -
Correspondance : 1 D = 3,336
× 10 –
30 C.m
-
En conséquence : p ≈ 1,60
× 10 –
29 C.m
≈ 4,8 D -
Le debye est une unité bien adaptée à
l’échelle de la molécule. -
Pour représenter le moment dipolaire
-
On peut utiliser l’échelle suivante : 2 D ↔ 1
cm -
Longueur du représentant : ℓp
≈ 2,4 cm
-
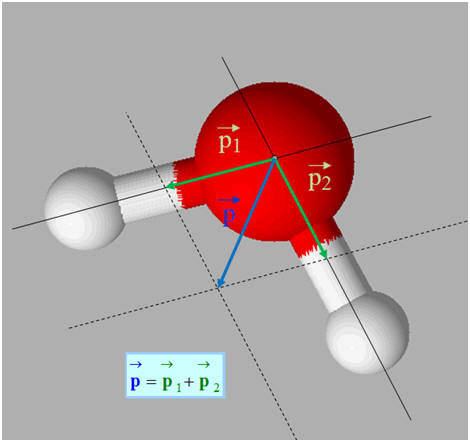
Moment dipolaire de la molécule d’eau : -
L’oxygène est plus électronégatif que
l’hydrogène. -
Les deux liaisons covalentes O – H
d’une molécule d’eau sont polarisées. -
Le moment dipolaire de la liaison O – H
est tel que p (H – O) = 1,5
D -
Le moment dipolaire résultant est égal à la
somme vectorielle des moments dipolaires des deux
liaisons O – H. -
Ainsi, on peut connaître le moment dipolaire
de la molécule d’eau : -
On trace le représentant de chaque vecteur
moment dipolaire de chaque liaison chimique. -
On utilise l’échelle : 2 cm ↔ 1 D. - Longueur du représentant : ℓ p1 = ℓ p2 = 3 cm -
On trace le vecteur du moment résultant
-
On mesure la valeur de la longueur du
représentant du vecteur : -
Schéma et mesures réalisées avec le logiciel
Word 2007. -
ℓp ≈ 3,7 cm. -
On en déduit que p (H2O)
≈ 1,85 D ≈ 1,9 D |
|
|
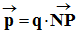
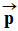 , il faut une échelle
, il faut une échelle 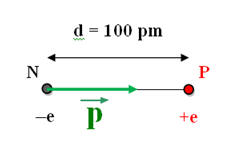

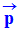 qui est égal à
la somme vectorielle de
qui est égal à
la somme vectorielle de