|
Chim N° 09 |
Synthèse d'espèces chimiques. Exercices. |
|
|
Mots clés : Cours de chimie seconde La réaction chimique, transformation physique, transformation chimique, système chimique, état initial, état final, lois de conservation, écriture d'une équation chimique, nombres stœchiométriques, effets termiques des trasformations physiques, effets thermiques des transformations chimiques, endothermique, exothermique, athermique, QCM, Vaporisation, fusion, solidification, sublimation, liquéfaction, effort physique, sueur, ... |
|
|
|
I- Exercice 3
page 282 : Connaître le matériel utilisé pour une synthèse.
II- Exercice 5
page 282 ; Nommer les étapes d’une synthèse. |
I- Exercice 3 page 282 : Connaître le matériel utilisé pour une synthèse.
|
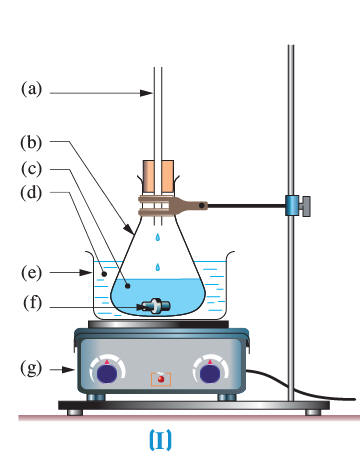
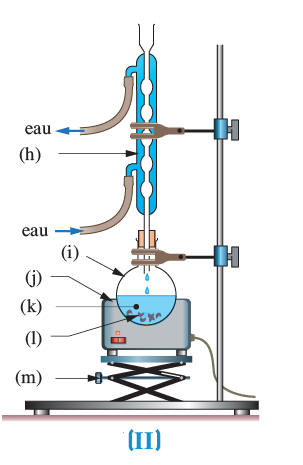
1)- Quel est l’intérêt du chauffage à reflux ? 2)- Comment le reflux est-il assuré ? 3)- Reproduire et légender les schémas ci-après :
4)- Qu’est-ce qui distingue les réfrigérants des montages (I) et (II) ? |
|
1)- Intérêt du chauffage à reflux : - Il permet de travailler à température élevée et ainsi d’accélérer la réaction chimique. - Il permet d’éviter les pertes de réactifs et de produits. - Les réactifs et les produits qui se vaporisent retombent dans le mélange réactionnel lorsqu’ils se condensent. 2)- Le reflux : - Il est assuré par le condenseur ou le réfrigérant qui permet de condenser les produits et les réactifs de la réaction. - Les produits et les réactifs de la réaction se retrouvent ainsi dans le mélange réactionnel. 3)- Les schémas et la légende :
4)- Les réfrigérants des montages (I) et (II) : - Montage (I) : réfrigérant à air : on utilise l’air ambiant pour refroidir les vapeurs formées (il faut utiliser un tube suffisamment long) - Montage (II) : réfrigérant à eau : on utilise l’eau pour refroidir les vapeurs formées. |
II- Exercice 5 page 282 ; Nommer les étapes d’une synthèse.
|
L’aspirine est obtenue en chauffant à reflux de l’acide salicylique (solide) et de l’anhydride acétique (liquide). Il se forme également de l’acide acétique. Après réaction, l’addition d’eau dans le mélange réactionnel transforme l’excès d’anhydride acétique en acide acétique (très soluble dans l’eau) et entraîne la formation de cristaux blancs que l’on récupère. Pour vérifier que ces cristaux contiennent bien de l’aspirine, on réalise une chromatographie sur couche mince avec un éluant adapté. 1)- Recopier les phrases du texte qui concernent : a)- L’étape de synthèse ; b)- L’étape de séparation ; c)- L’étape d’identification. 2)- Quelle opération aurait-il été préférable d’effectuer avant l’étape d’identification ? |
|
3=1)- Les phrases du texte : a)- Étape de Synthèse : - « L’aspirine est obtenue en chauffant à reflux de l’acide salicylique (solide) et de l’anhydride acétique (liquide). Il se forme également de l’acide acétique ». b)- Étape de séparation : - « Après réaction, l’addition d’eau dans le mélange réactionnel transforme l’excès d’anhydride acétique an acide acétique (très soluble dans l’eau) et entraîne la formation de cristaux blancs que l’on récupère ». c)- Étape d’Identification : - « Pour vérifier que ces cristaux contiennent bien de l’aspirine, on réalise une chromatographie sur couche mince avec un éluant adapté ». 2)- Opération à d’effectuer avant l’étape d’identification : - Il aurait fallu effectuer une purification avant l’identification : dans le cas présent, il s’agit d’une recristallisation. - Le but de cette manipulation est de purifier l’acide acétylsalicylique en utilisant la différence de solubilité entre un corps et ses impuretés dans un solvant. - On dissout l’acide acétylsalicylique impur à chaud dans un solvant approprié (éthanol). - Lorsque la solution refroidit, l’aspirine cristallise et les impuretés restent en solution
-
L’acide
acétylsalicylique impur et 6 mL d’éthanol.
-
Chauffer au bain-marie
en agitant jusqu’à dissolution complète du solide.
-
Ajouter 15 mL d’eau
distillée à la température ambiante.
-
Laisser refroidir à
température ambiante, puis placer l’erlenmeyer dans
un bain eau – glace (stabiliser avec le lest). - Filtrer sur Büchner, sécher et peser : |
III- Exercice 9 page 284 : Le baume du Pérou.
|
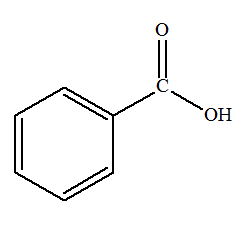
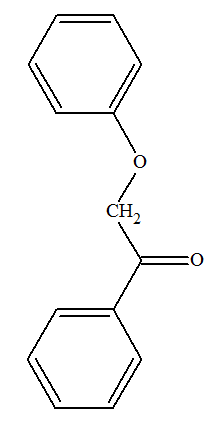
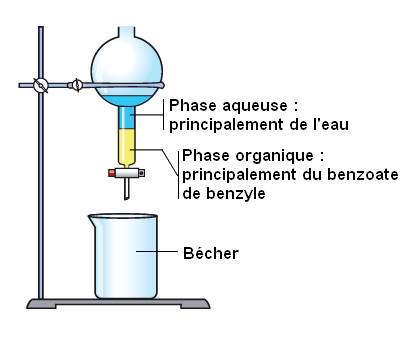
Le baume du Pérou est extrait d’un arbuste d’Amérique centrale, le myroxylon, après incision de l’écorce de son tronc. Utilisé pour traiter les gerçures et engelures, il a des propriétés protectrices et hydratantes. Il contient, entre autres, de l’acide benzoïque, de l’alcool benzylique et du benzoate de benzyle.
1)- Le benzoate de benzyle peut être synthétisé à partir de l’alcool benzylique et de l’acide benzoïque. Écrire l’équation de cette réaction, sachant qu’il se forme aussi de l’eau. 2)- On réalise la synthèse en utilisant un chauffage à reflux. a)- Schématiser et légender le montage. Indiquer le sens de circulation de l’eau dans le réfrigérant. b)- Quel est l’intérêt de ce montage ? 3)- Après 20 min, on refroidit le ballon puis on verse le contenu dans une ampoule àdécanter contenant de l’eau salée. Après agitation puis décantation, on observe deux phases non miscible. a)- Quel est l’intérêt de cette dernière étape ? b)- Décrire, avec précision, les différentes opérations effectuées lors de l’utilisation de l’ampoule à décanter. c)- Schématiser l’ampoule à décanter et indiquer les positions de la phase aqueuse et de la phase organique, contenant, entre autres, le benzoate de benzyle. 4)- On réalise une chromatographie sur couche mince. Les dépôts sont les suivants : - En A : alcool benzylique ; - En B : benzoate de benzyle ; - En C : un échantillon du liquide de synthèse ; - En D un extrait de résine de myroxylon. a)- Sur le chromatogramme représenté ci-après, identifier dans les dépôts C et D la tache correspondant au benzoate de benzyle. b)- Le dépôt effectué en C est-il celui d’un produit pur ? c)- Indiquer la composition de l’échantillon C. d)- Identifier deux espèces présentes dans la résine de myroxylon. Justifier.
|
|
1)- Équation bilan de la réaction chimique :
C7H8O
+
C7H6O2
→
C14H12O2
+
H2O
2)- Chauffage à reflux : a)- Schéma légendé :
b)- Intérêt du montage : le chauffage à reflux : - Il permet de travailler à température élevée et ainsi d’accélérer la réaction chimique. - Il permet d’éviter les pertes de réactifs et de produits. - Les réactifs et les produits qui se vaporisent retombent dans le mélange réactionnel lorsqu’ils se condensent. 3)- Utilisation d’une ampoule à décanter : a)- Intérêt de cette dernière étape : - Cette étape permet d’extraire le benzoate de benzyle de la phase aqueuse. - Le benzoate de benzyle est moins soluble dans l’eau salée que dans l’eau. - On refroidit aussi car la solubilité dans l’eau diminue avec la température. b)- Les différentes opérations effectuées : - On verse le mélange réactionnel dans une ampoule à décanter qui est placé sur son support et sous laquelle on a placé un bécher ou un verre à pied (ne pas oublier de fermer le robinet de l’ampoule à décanter) - Saisir l’ampoule à décanter tout en maintenant le bouchon. La retourner et ouvrir le robinet. - Agiter. Fermer le robinet, placer l’ampoule à décanter sur son support et laisser décanter. c)- Schéma de l’ampoule à décanter :
4)- Chromatographie : a)- Identification : - Tache qui correspond au benzoate de benzyle :
b)- Dépôt C : - Le dépôt C n’est pas un corps pur car après élution, on obtient deux taches. - C’est un mélange d’au moins deux espèces chimiques. c)- Composition de l’échantillon C : - Le dépôt C contient du benzoate de benzyle et de l’alcool benzylique. d)- Identification de deux espèces présentes dans la résine de myroxylon : - La résine de myroxylon contient, entre autres : - Du benzoate de benzyle car on observe une tache au même niveau que celle du dépôt B qui est du benzoate de benzyle. - De l’alcool benzylique car on observe une tache au même niveau que celle du dépôt A qui est de l’alcool benzylique. |
IV- Exercice 13 page 286 : Les texticaments.
|
Une coudière qui délivre en continu un anti-inflammatoire pour un tennisman souffrant d’un tennis-elbow ? Pourquoi pas ! Crèmes hydratantes, huiles essentielles, antibiotiques… tout est encapsulable : Le principe actif est enfermé dans une membrane en matière plastique (en Nylon ® par exemple – doc1). Le vêtement devient un patch géant à porter toute la journée ! Des milliards de microcapsules mesurant de un à quelques micromètres sont fixées aux fibres par un liant et diffusent leur contenu sous l’effet des frottements du textile sur la peau. (doc.2)
1)- Pourquoi qualifie-t-on certains textiles de texticaments ? 2)- Comment le principe actif contenu dans la capsule est-il libéré ? 3)- Pourquoi parle-t-on de microcapsule ? 4)- Dans l’exemple choisi, quelle est l’espèce chimique qui constitue la paroi de la capsule ? 5)- Quels sont les réactifs qui réagissent lors de la fabrication de la microcapsule précédente ? |
|
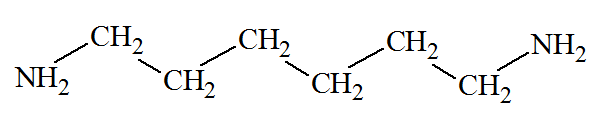
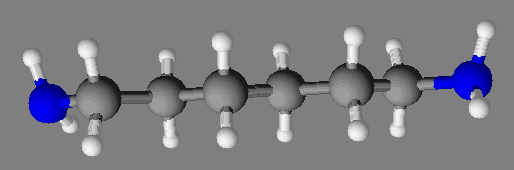
1)- Ce terme résulte de la contraction des deux termes : textile, médicament. C’est un néologisme. 2)- Libération du principe actif : - « Les microcapsules …diffusent leur contenu sous l’effet des frottements du textile sur la peau » - Le principe actif est libéré par frottement du vêtement sur la peau. 3)- Microcapsules : - La taille des capsules est de l’ordre du micromètre. 4)- Les réactifs pour la fabrication des capsules : - Les réactifs de la synthèse des microcapsules sont : - L’hexane -1,6-diamine - Le chlorure de sébacoyle (c'est un chlorure d'acyle qui sert à la fabrication du Nylon 6,10) Cliquer sur l'image pour l'agrandir |
|
|