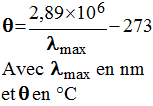|
Pour s'auto-évaluer |
Sources de lumières, couleurs et photons |
|
|
|
|
QCM N° 03 Sources de lumières,
couleurs et photons.
Pour chaque question, indiquer la (ou les)
bonne(s) réponse(s).
|
|||||
|
|
Énoncé |
A |
B |
C |
R |
|
1 |
Quelle (s) spectre(s) correspond(ent) à la lumière d’une source polychromatique ? |
|
|
|
BC |
|
2 |
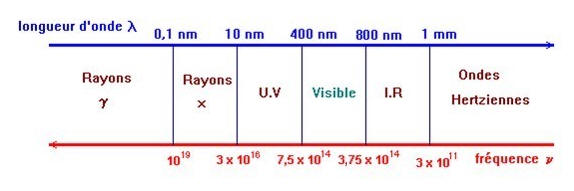
Les radiations infrarouges ont, dans le vide, des longueurs d’onde λ : |
Inférieures à
400 nm |
Supérieures à
800 nm |
Inférieures à celles des radiations rouges |
B |
|
3 |
Une source froide telle qu’une DEL émet de la lumière : |
Sans échauffement particulier |
Par absorption de photons |
Par émission de
photons |
AC |
|
4 |
Plus un corps est chaud, plus son spectre s’enrichit de radiations : |
Infrarouges |
De grandeurs longueurs d’onde |
De courtes longueurs d’ondes |
C |
|
5 |
On donne la loi de Wien :
La radiation émise avec un maximum d’intensité par une source lumineuse a pour longueur d’onde dans le vide λ max = 700 nm. Sa température de surface est d’environ : |
3,86
× 103
° C |
4,40
× 103
° C |
4,13
× 105
° C |
A |
|
6 |
Le spectre ci-dessous a été obtenu avec du sodium. La présence de la raie
traduit :
|
L’absorption de
photons |
L’émission d’électrons |
L’émission de
photons |
C |
|
7 |
L’énergie d’un photon de longueur d’onde dans le vide λ = 450 nm vaut : On donne : c = 3,00
× 10
8
m / s et La constante de Planck : h = 6,63 × 10 – 34 J . s |
4,42
× 10
– 19 J |
4,42
× 10
– 28 J |
4,42
× 10
– 18 J |
A |
|
8 |
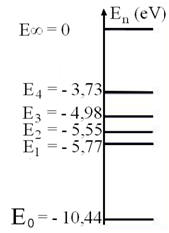
On donne une partie du diagramme de niveaux d’énergie du mercure. Les atomes de mercure pris dans leur état fondamental peuvent absorber un photon d’énergie :
|
4,67 eV |
3,73 eV |
2 ,04 eV |
A |
|
9 |
Quelle est la longueur d’onde λ d’un photon d’énergie 4,67 eV ? 1 eV = 1,6
× 10
– 19 J |
405 nm |
266 nm |
2,66
× 10
– 7 m |
BC |
|
10 |
À partir du profil spectral du Soleil, la loi de Wien permet de connaître : |
Sa température de surface |
La composition de son atmosphère |
Sa masse |
A |
|
11 |
Les entités chimiques présentes dans l’atmosphère du Soleil sont identifiées à
partir : |
De sa température |
Des raies noires du spectre solaire |
Des minima d’intensité lumineuse de son profil spectral |
BC |
|
12 |
Une lumière colorée : |
Est toujours monochromatique |
Est toujours polychromatique |
Peut être l’une ou l’autre selon le cas |
C |
|
13 |
Les radiations ultraviolettes ont une longueur d’onde dans le vide : |
Inférieure à 400
nm |
Supérieure à 800
nm |
Comprise entre 400 nm et 800 nm |
A |
|
14 |
Deux lumières colorées qu’un observateur perçoit identiques : |
Ont obligatoirement des spectres identiques |
Peuvent avoir des spectres différents |
Ont obligatoirement la même longueur d’onde |
B |
|
15 |
La loi de Wien montre que si la température d’un corps augmente, la longueur d’onde du maximum d’émission :
|
Augmente |
Diminue |
Ne varie pas |
B |
|
16 |
Si la température d’un corps augmente, son spectre d’émission : |
S’agrandit vers les courtes longueurs d’onde |
S’agrandit vers les grandes longueurs d’onde |
N’est pas
modifié |
A |
|
17 |
La couleur d’un corps chauffé : |
Dépend de l’ensemble des radiations qu’il émet |
Dépend exclusivement de la longueur d’onde de son maximum d’émission |
Passe du jaune au rouge si sa température augmente |
A |
|
18 |
La fréquence d’une radiation de longueur d’onde dans le vide λ = 550 nm a pour
valeur : |
5,45
× 105
Hz |
5,45
× 1014
Hz |
3,61
× 10–19
Hz |
B |
|
19 |
L’unité S.I de la constante de Planck est : |
J / s |
J . s |
s / J |
B |
|
20 |
L’énergie d’un photon d’une radiation de lumière violette : |
Est supérieure à celle d’une radiation de lumière rouge |
Est supérieure à celle d’une radiation UV |
Augmente avec l’intensité de la source |
A |
|
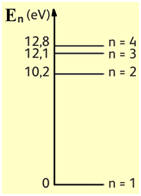
21 |
D’après le diagramme d’énergie de l’atome d’hydrogène donné ci-dessous, l’énergie d’un atome d’hydrogène, initialement dans son état fondamental, peut être modifiée par absorption D’un photon d’énergie :
|
10,4 eV |
12,1 eV |
5,1 eV |
B |
|
22 |
Les raies sombres du spectre solaire sont dues essentiellement à l’absorption de
la lumière par :
|
La photosphère |
La chromosphère |
L’atmosphère terrestre |
B |
►
Source polychromatique :
-
Une lumière polychromatique est
une lumière constituée de plusieurs couleurs ou radiations.
-
La lumière blanche est constituée
de plusieurs couleurs ou radiations : c’est une lumière
polychromatique.
►
Source
monochromatique :
-
Une lumière monochromatique est
une lumière constituée d’une seule couleur ou radiation.
-
Elle est caractérisée par:
-
Sa fréquence
ν (en Hz) ou sa période
T (en s).
-
Sa longueur d’onde dans le vide
λ0.
-
La lumière produite par un laser
est constituée d’une seule radiation, elle est monochromatique.
►
Radiations
infrarouges :
-
Les radiations infrarouges ont, dans le vide, des longueurs
d’onde supérieures à 800 nm : λ0 >
800 nm.
►
Les radiations
ultraviolettes :
-
Les radiations ultraviolettes ont une longueur d’onde dans le
vide inférieure à 400 nm : λ0 < 400 nm.
►
Spectre d’émission :
- Un spectre d’émission est un spectre produit par la lumière directement émise par une source.
- Un spectre lumineux est la figure obtenue par décomposition d’une lumière complexe en ses radiations lumineuses.
- Les spectres continus d’origine thermique.
- Exemples : la lampe à incandescence dont on augmente la valeur de la tension.
- Tout corps chauffé à une température suffisante émet de la lumière.
- Le spectre de la lumière émise par un corps chauffé est un spectre d’origine thermique.
- Le corps peut être un solide, un liquide que l’on chauffe ou un gaz fortement comprimé.
►
Les spectres d’origine
thermique.
-
Les spectres d’origine thermique
sont des spectres continus.
- Le spectre évolue avec la température.
- Lorsque la température augmente, le spectre devient de plus en plus lumineux et s’enrichit de couleurs vertes, bleues puis violettes.
- Il s’étale vers les violets et ultraviolets. Il s‘étale vers les courtes longueurs d’onde.

►
Les spectres de raies.
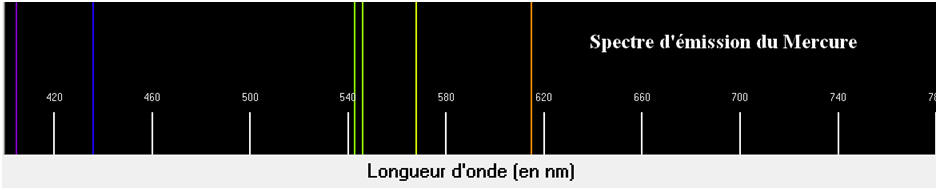
- Exemple : la lampe à vapeur de mercure.
- La lampe contient des atomes de mercure sous faible pression. On excite les atomes de mercure grâce à des décharges électriques.
- Observations : le spectre obtenu est discontinu. Il est constitué d’un nombre limité de radiations.
- Conclusion : un gaz, à faible pression et à température élevée, émet une lumière constituée d’un nombre limité de radiations. On obtient un spectre de raies.
- Le spectre obtenu est caractéristique des atomes du gaz qui émet les radiations.
- Un spectre de raies constitue la signature d’un élément chimique et révèle sa présence. Il permet d’identifier une entité chimique (atome ou ion).
►
Les spectres d’absorption.
- Un spectre d’absorption est un spectre obtenu en analysant la lumière blanche qui a traversé une substance.
►
Spectres de raies
d’absorption.
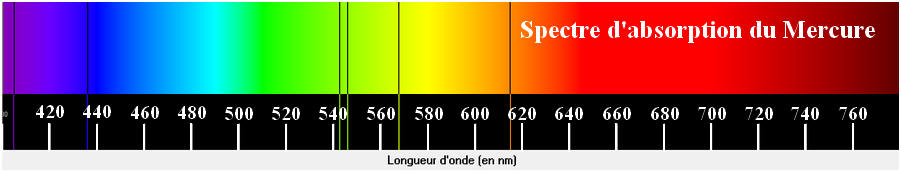
- Un gaz, à basse pression et à basse température, traversé par une lumière blanche, donne un spectre d’absorption.
- Ce spectre est constitué de raies noires se détachant sur le fond coloré du spectre de la lumière blanche.
- Ce spectre est caractéristique de la nature chimique d’un atome ou d’un ion.
- Exemple : spectre de raies d’absorption du mercure :
Comparaisons des spectres
d'absorption et
►
Spectre d’émission d’une entité chimique :
-
Le spectre d’émission d’une
entité chimique est constitué de raies colorées sur fond noir.
On est en présence d’un spectre de raies.
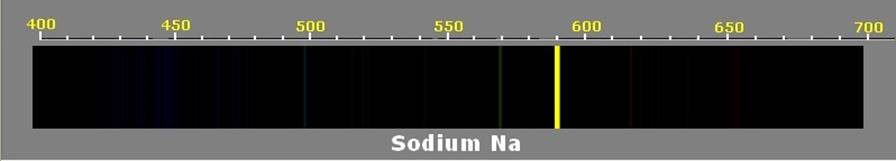
-
Spectre de la lampe à vapeur de
sodium :
-
Le doublet du sodium : radiations
jaunes de longueur d’onde voisine de 590 nm (en réalité, il
s’agit d’un doublet : 589,0 nm et 589,6 nm)
►
Loi de Wien :
-
Un corps chaud émet de la lumière
dont le spectre et le profil spectral dépendent de la
température.
-
En physique, un « corps noir »
est un objet idéal émettant un rayonnement qui n’est fonction
que de sa température.
-
La loi de Wien relie la
température θ de ce corps noir et la longueur d’onde λ
max pour laquelle le profil spectral de la
lumière qu’il émet passe par un maximum.
-
La température θ s’exprime
en degré Celsius et la longueur d’onde λ max
en nm.
-
Ces deux grandeurs sont liées par
la loi de Wien :
-
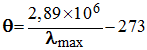
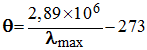
-
Cette loi permet d’évaluer la
température d’une étoile à partir de son profil spectral.
-
Sa température de surface est d’environ :
-
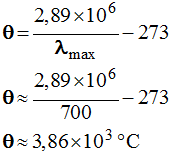
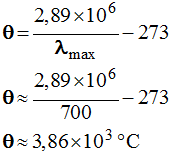
►
La chromosphère :
-
On appelle chromosphère
l’atmosphère située autour du Soleil. Son épaisseur est de
l’ordre de 2000 km environ.
- Cette atmosphère est constituée de gaz sous faible pression avec des régions où la température atteint 104 ° C.
►
Spectre de la lumière émise par le
soleil :
- C’est un spectre continu présentant des raies d'absorptions.
- L’atmosphère du Soleil contient des éléments chimiques.
- La partie haute de l’atmosphère absorbe une partie de la lumière émise dans la partie basse.
- Il en résulte des raies d’absorption dans le spectre continu.
- Ce sont les raies d’absorption des éléments chimiques présents dans l’atmosphère du Soleil.
- L’existence des raies d’absorption est dû à la présence d’une atmosphère autour du Soleil, appelée chromosphère.
- Le gaz présent est principalement de l’hydrogène.
- On trouve aussi des ions He+, Ca2+, Fe2+, …
►
Propriétés des ondes lumineuses.
- Les ondes lumineuses possèdent :
- Une vitesse de propagation ou célérité qui dépend du milieu de propagation.
- La lumière se déplace dans le vide à la vitesse : c = 3,00 × 108 m / s .
- Dans un milieu transparent d’indice n :
-
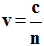 avec n > 1.
avec n > 1.
- Une périodicité temporelle T, la période en seconde s.
- Une périodicité spatiale λ, la longueur d’onde en mètre m.
- à un instant donné, les signaux sont dans le même état vibratoire s’ils sont placés à des distances d, d + λ, d + n.λ de la source.
►
Relation fondamentale.
-
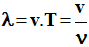 ;
;
- λ est la longueur d’onde en m
- v est la vitesse de l’onde dans le milieu de propagation et T la période en s.
- ν est la fréquence en Hz
- Remarque :
-
dans le vide : λ0
= c . T
- Dans le milieu d’indice n,
-
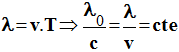
- La longueur d’onde dépend du milieu de propagation.
-
La période et de ce fait la
fréquence ne dépendent pas du milieu de propagation.
- La fréquence ν est une grandeur caractéristique de la radiation lumineuse.
►
Énergie d’un
photon :
-
E = h . ν ou
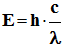
-
Pour une onde électromagnétique
de fréquence ν et de longueur d’onde λ dans le vide
-
La grandeur h est la
constante de Planck : h = 6,63
× 10
– 34 J.s.
-
La grandeur c représente la
valeur de la vitesse de la lumière dans le vide :
-
c = 3,00
× 10 8 m / s
-
L’énergie E s’exprime en joule.
- Comme les valeurs des énergies des atomes, exprimées en joule (J) sont extrêmement faibles,
- on
préfère utiliser le plus souvent comme unité d’énergie,
l’électron-volt (eV)
-
Correspondance : 1 eV = 1,6
× 10 –
19 J
-
L’énergie d’un photon de longueur
d’onde dans le vide λ = 450 nm vaut :
-


►
Variations
d’énergie d’un atome :
-
En 1913, BOHR énonce les
postulats suivants :
-
Les variations d’énergie d’un
atome sont quantifiées.
-
L’atome ne peut exister que dans
certains états d’énergie ou niveaux d’énergie bien définis.
-
Un photon de fréquence ν
est émis lorsque l’atome effectue une transition d’un niveau
d’énergie Ep vers un niveau inférieur En
tel que :
- Les variations d’énergie d’un atome sont quantifiées.
- L’atome ne peut exister que dans certains états d’énergie ou niveaux d’énergie bien définis.
- Un photon de fréquence ν est émis lorsque l’atome effectue une transition d’un niveau d’énergie Ep vers un niveau inférieur En tel que :
-
Ep - En
= h . ν
-
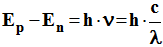
►
Longueur d’onde
d’un photon :
-
E = h . ν
-
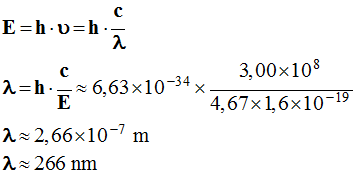
►
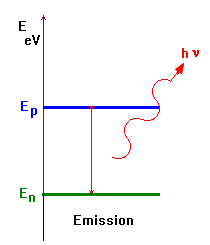
Émission d’un
photon :
-
Un photon de fréquence ν
est émis lorsque l’atome effectue une transition d’un niveau
d’énergie Ep vers un niveau inférieur En
tel que :
►
Absorption d’un
photon :
- L’absorption d’énergie lumineuse par un atome ne peut se faire que si l’énergie du photon permet une transition d’un niveau En à un niveau supérieur Ep tel que :
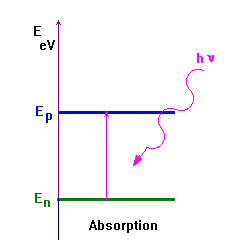
-
Ep - En
= h . ν
- Un atome ne peut absorber que les radiations qu’il est capable d’émettre.
►
Relation
fondamentale :
-
La longueur d’onde dans le vide
d’une radiation lumineuse est donnée par la relation :
-


-
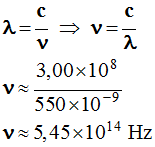
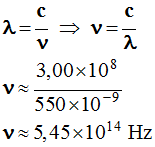
|
|